神经源性炎症 NI或NI是生理过程,其中介质直接从皮肤神经排出,开始发生炎症反应。 这导致局部炎症反应的产生,包括红斑,肿胀,体温升高,压痛和疼痛。 对低强度机械和化学刺激有反应的细无髓传入体C纤维在很大程度上负责这些炎症介质的释放。
受到刺激时,皮神经中的这些神经通路会释放出高能神经肽或P物质和降钙素基因相关肽(CGRP),迅速进入微环境,引发一系列炎症反应。 免疫原性炎症有一个明显的区别,那就是当病原体进入人体时免疫系统做出的第一个保护性和修复性反应,而神经源性炎症则涉及神经系统和炎症性反应之间的直接联系。 即使神经源性炎症和免疫性炎症可以同时存在,但两者在临床上并不是无法区分的。 以下文章的目的是讨论神经原性炎症的机制以及外周神经系统在宿主防御和免疫病理学中的作用。
内容
神经源性炎症-周围神经系统在宿主防御和免疫病理学中的作用
抽象
传统上认为外周神经和免疫系统具有独立的功能。 然而,由于对神经源性炎症的新见解,这条线变得越来越模糊。 伤害感受神经元具有与免疫细胞相同的许多危险分子识别途径,并且在对危险作出反应时,周围神经系统直接与免疫系统进行通讯,从而形成了完整的保护机制。 周围组织中感觉神经和植物神经纤维的密集神经支配网络以及高速的神经传导允许对免疫力进行快速的局部和全身性神经调节。 周围神经元在自身免疫和过敏性疾病的免疫功能障碍中也似乎起着重要作用。 因此,了解周围神经元与免疫细胞的协同相互作用可能会促进治疗方法,以增加宿主防御和抑制免疫病理学。
介绍
两千年前,塞尔苏斯(Celsus)将炎症定义为涉及四个基本体征-Dolor(疼痛),卡路里(热),Rubur(发红)和肿瘤(肿胀),这一观察表明神经系统的激活被认为是神经系统不可或缺的一部分。炎。 但是,从那时起,人们一直主要考虑疼痛,只是作为一种症状,而不是炎症的参与者。 从这个角度来看,我们表明外周神经系统在调节先天和适应性免疫中起着直接和积极的作用,因此免疫和神经系统在宿主防御和对组织损伤的反应中可能具有共同的整合保护功能,这是一个复杂的过程。相互作用还可能导致变态反应性和自身免疫性疾病的病理。
有机体的生存至关重要地取决于对防御来自组织破坏和感染的潜在危害进行防御的能力。 宿主防御既包括避免行为以消除与危险(有害)环境的接触(神经功能),也包括主动中和病原体(免疫功能)。 传统上,人们认为免疫系统在抵抗传染病和修复组织损伤中的作用与神经系统完全不同,后者将破坏性的环境和内部信号转化为电活动,从而产生感觉和反射(图1)。 我们建议这两个系统实际上是统一防御机制的组成部分。 体感神经系统是放置危险的理想选择。 首先,所有高度暴露于外部环境的组织,例如皮肤,肺,泌尿和消化道的上皮表面,都受到伤害感受器和产生疼痛的高阈值感觉纤维的密集支配。 其次,有害外部刺激的传导几乎是瞬时的,比先天免疫系统的动员快几个数量级,因此可能是宿主防御中的``第一反应者''。
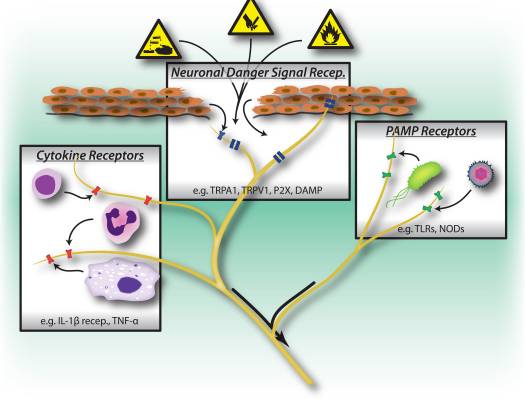
图1: 有害刺激,微生物和炎症识别途径触发周围神经系统的激活。 感觉神经元具有几种检测有害/有害刺激物存在的方法。 1)危险信号受体,包括TRP通道,P2X通道和危险相关分子模式(DAMP)受体,可以识别环境中的外源信号(例如热,酸度,化学物质)或创伤/组织损伤期间释放的内源性危险信号(例如ATP,尿酸,羟基壬烯)。 2)模式识别受体(PRR),例如Toll样受体(TLR)和Nod样受体(NLR),可以识别感染过程中细菌或病毒入侵所致的病原相关分子模式(PAMP)。 3)细胞因子受体识别免疫细胞分泌的因子(例如IL-1beta,TNF-α,NGF),这些因子激活图谱激酶和其他信号传导机制以增加膜的兴奋性。
除了从周围向脊髓和大脑输入正畸学外,伤害感受器神经元中的动作电位还可以在分支点处反抗地传递到周围,即轴突反射。 这些与持续的局部去极化一起导致神经介质从周围轴突和末端快速和局部释放(图2)1. Goltz(1874年)和Bayliss(1901年)的经典实验表明,电刺激背根诱导皮肤血管舒张,从而导致了``神经源性炎症''的概念,与免疫系统产生的炎症无关(图3)。
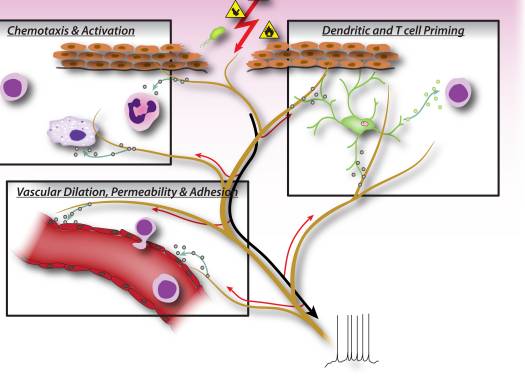
图2: 从伤害感受器感觉神经元释放的神经元因子直接驱动白细胞趋化性,血管血流动力学和免疫反应。 当有害刺激激活感觉神经中的传入信号时,就会产生抗皮层轴突反射,从而诱导神经元外围末端神经肽的释放。 这些分子介质具有几种炎性作用:1)中性粒细胞,巨噬细胞和淋巴细胞的趋化性和活化至损伤部位,肥大细胞脱粒。 2)向血管内皮细胞发出信号以增加血流量,血管渗漏和水肿。 这也使炎症性白细胞的募集更加容易。 3)引发树突状细胞以驱动随后的T辅助细胞分化为Th2或Th17亚型。

图3: 从Celsus到今天,了解炎症的神经源性方面进展的时间表。
神经源性炎症由伤害感受器释放神经肽降钙素基因相关肽 (CGRP) 和 P 物质 (SP) 介导,它们直接作用于血管内皮细胞和平滑肌细胞 2�5。 CGRP 产生血管舒张作用 2、3,而 SP 增加毛细血管通透性导致血浆外渗和水肿 4、5,导致 Celsus 的红肿、热量和肿瘤。 然而,伤害感受器会释放许多额外的神经肽(在线数据库: www.neuropeptides.nl/),包括肾上腺髓质素、神经激肽 A 和 B、血管活性肠肽 (VIP)、神经肽 (NPY) 和胃泌素释放肽 (GRP),以及其他分子介质,如谷氨酸、一氧化氮 (NO) 和细胞因子,如 eotaxin 6.
我们现在意识到从周围感觉神经元释放的介体不仅作用于脉管系统,而且还直接吸引并激活先天免疫细胞(肥大细胞,树突状细胞)和适应性免疫细胞(T淋巴细胞)7-12。 在组织损伤的急性环境中,我们推测神经源性炎症是保护性的,通过激活和募集免疫细胞促进生理性伤口愈合和针对病原体的免疫防御。 但是,通过放大病理或适应不良的免疫反应,这种神经免疫通讯也可能在变应性和自身免疫性疾病的病理生理中起主要作用。 例如,在类风湿性关节炎的动物模型中,Levine及其同事发现关节的神经支配导致炎症显着减弱,这取决于P 13、14物质的神经表达。牛皮癣,主要的感觉神经元在启动和增强先天性和适应性免疫的激活中起着中心作用15-17。
因此,我们建议,外周神经系统不仅在宿主防御中起被动作用(有害刺激的检测和逃避行为的启动),而且在调节免疫系统对有害物质的反应和与之作斗争中还起着与免疫系统协同作用的作用。刺激,这种作用可以被颠覆以促成疾病。
周围神经和先天免疫系统中的共享危险识别途径
外围感觉神经元因其对强烈的机械,热和刺激性化学刺激的敏感性而适于识别对机体的危险(图1)。 瞬态受体电位(TRP)离子通道是伤害感受最广泛研究的分子介质,在受到各种有害刺激激活后会进行阳离子的非选择性进入。 TRPV1被高温,低pH和辣椒素活化,辣椒素是辣椒18的类缬氨酸刺激成分。TRPA1介导检测反应性化学物质,包括催泪气体和工业异硫氰酸盐19等环境刺激性物质,但更重要的是,它在组织过程中也被激活内源性分子信号引起的损伤,包括4-羟基壬烯醛和前列腺素20、21。
有趣的是,感觉神经元与先天免疫细胞共享许多相同的病原体和危险分子识别受体途径,这使它们也能够检测病原体(图1)。 在免疫系统中,微生物病原体由种系编码的模式识别受体(PRR)检测,该受体识别广泛保守的外源病原体相关分子模式(PAMP)。 首先要鉴定的PRR是Toll样受体(TLR)家族的成员,该家族与酵母,细菌衍生的细胞壁成分和病毒RNA 22结合。适应性免疫。 除TLR外,组织损伤期间先天性免疫细胞还通过内源性衍生危险信号(也称为损害相关分子模式(DAMP)或警报蛋白23、24)激活。这些危险信号包括HMGB1,尿酸和释放的热休克蛋白通过在坏死过程中使细胞死亡,在非感染性炎症反应过程中激活免疫细胞。
伤害感受器神经元表达包括TLR 3、4、7和9的PRR,TLR配体刺激导致感应电流流入,伤害感受器对其他疼痛刺激敏感25-27。 此外,TLR7配体咪喹莫特对感觉神经元的激活导致瘙痒特异性感觉途径25的激活。这些结果表明,与感染相关的疼痛和瘙痒可能部分归因于病原体衍生因子对神经元的直接激活。通过神经元信号分子的外围释放来激活免疫细胞。
细胞损伤期间释放的主要DAMP /阿拉明是ATP,在伤害感受器神经元和免疫细胞28‐30上的嘌呤能受体都可以识别ATP。 嘌呤能受体由两个家族组成:P2X受体,配体门控的阳离子通道和P2Y受体,G蛋白偶联受体。 在伤害感受器神经元中,ATP的识别通过P2X3发生,从而导致阳离子电流迅速致敏并引起疼痛28、30(图1),而P2Y受体通过TRP和电压门控钠通道的致敏作用促进伤害感受器的激活。 在巨噬细胞中,ATP与P2X7受体的结合会导致超极化和炎症小体的下游激活,炎症小体是在产生IL-1beta和IL-18时很重要的分子复合物29。因此,ATP是激活周围神经元和先天性神经的有效危险信号。受伤时具有免疫力,甚至有证据表明神经元表达了炎性分子分子机制的一部分31。
伤害感受器中危险信号的另一面是TRP通道在免疫细胞激活中的作用。 TRPV2是由有害热激活的TRPV1的同源物,在先天免疫细胞中高水平表达32。TRPV2的遗传切除导致巨噬细胞吞噬作用和细菌感染清除的缺陷32.肥大细胞还表达TRPV通道,可直接介导它们的脱粒作用33.内源性危险信号是否像伤害感受器一样激活免疫细胞还有待确定。
免疫细胞和伤害感受器神经元之间进行交流的关键手段是通过细胞因子。 细胞因子受体激活后,感觉神经元中的信号转导通路被激活,导致膜蛋白的下游磷酸化,包括TRP和电压门控通道(图1)。 由此产生的伤害感受器敏化意味着通常无害的机械刺激和热刺激现在可以激活伤害感受器。 白细胞介素1β和TNF-α是炎症过程中先天免疫细胞释放的两种重要细胞因子。 表达相关受体的伤害感受器直接感应到IL-1beta和TNF-α,诱导p38映射激酶激活,从而导致膜兴奋性增强34-36。 神经生长因子(NGF)和前列腺素E(2)也是从免疫细胞释放的主要炎症介质,直接作用于周围感觉神经元以引起敏化。 免疫因子对伤害感受器致敏作用的重要作用是增加了外围肽中神经肽的释放,从而进一步激活了免疫细胞,从而诱导了正反馈回路,从而驱动并促进炎症。
先天和适应性免疫的感觉神经系统控制
在炎症的早期,感觉神经元会向组织中的肥大细胞和树突状细胞发出信号,它们是先天免疫细胞,对启动免疫反应至关重要(图2)。 解剖学研究表明,肥大细胞以及树突状细胞直接与末端并列,从伤害感受器释放的神经肽可以诱导这些细胞7、9、37中的脱颗粒或细胞因子生成。这种相互作用在过敏性气道中起重要作用炎症和皮炎10 12。
在炎症的效应阶段,免疫细胞需要找到通往特定损伤部位的途径。 从感觉神经元,神经肽,趋化因子和谷氨酸释放的许多介体对嗜中性粒细胞,嗜酸性粒细胞,巨噬细胞和T细胞具有趋化作用,并增强内皮粘附,从而促进免疫细胞归巢6、38(图41)。 此外,一些证据表明神经元可能直接参与效应物阶段,因为神经肽本身可能具有直接的抗菌功能2。
通过促进不同类型的适应性免疫T细胞的分化或特异性,神经元来源的信号分子也可以指导炎症的类型。 抗原被先天免疫细胞吞噬并加工,然后迁移到最近的淋巴结并将抗原肽呈递给幼稚的T细胞。 根据抗原的类型,先天免疫细胞上的共刺激分子以及特定细胞因子的组合,幼稚T细胞会成熟为特定亚型,最能发挥炎症作用以清除病原刺激。 CD4 T细胞或T辅助(Th)细胞可分为四个原理组,即Th1,Th2,Th17和T调节细胞(Treg)。 Th1细胞主要参与调节对细胞内微生物和器官特异性自身免疫性疾病的免疫反应。 Th2对抵抗细胞外病原体(例如蠕虫)的免疫力至关重要,并且是过敏性炎症性疾病的原因。 Th17细胞在抵抗微生物挑战(例如细胞外细菌和真菌)方面发挥着重要作用; Treg细胞参与维持自我耐受和调节免疫反应。 这种T细胞的成熟过程似乎受到感觉神经元介体的严重影响。 神经肽,例如CGRP和VIP,可以通过促进某些细胞因子的产生和抑制其他细胞因子,以及减少或增强树突状细胞向局部淋巴结的迁移而使树突状细胞偏向Th2型免疫,并降低Th1型免疫。8 ,10,43.感觉神经元也对过敏性反应(主要是Th2驱动的炎症)做出了重要的贡献17。除了调节Th1和Th2细胞外,其他神经肽,例如SP和Hemokinin-1,可以使炎症反应更趋向于Th17或Treg。 44、45,这意味着神经元也可能参与调节炎症消退。 在结肠炎和牛皮癣等免疫病理学中,对神经元介质(如P物质)的阻滞可能会显着抑制T细胞和免疫介导的损伤15-17,尽管拮抗一种介质本身可能仅对神经源性炎症产生有限的影响。
考虑到从周围感觉神经纤维释放的信号分子不仅调节小血管,而且还调节免疫细胞的趋化性,归巢,成熟和激活,因此很明显,神经-免疫相互作用比以前认为的要复杂得多(图2)。 此外,完全可以想象的是不是影响伤害反应的不同阶段和类型的不是伤害感受器释放的信号分子的具体组合,而是个别神经介质的作用。
免疫的自主反射控制
胆碱能自主神经系统的“反射”回路在调节外周免疫反应中的作用也很突出46。迷走神经是连接脑干和内脏器官的主要副交感神经。 凯文·特雷西(Kevin Tracey)等人的研究指出,在迷走神经的传出刺激导致外周巨噬细胞受到抑制的情况下,在败血性休克和内毒素血症中存在强效的全身性抗炎反应47。 迷走神经激活支配脾脏的周围肾上腺能力腹腔神经节神经元,导致乙酰胆碱的下游释放,乙酰胆碱与脾脏和胃肠道巨噬细胞上的α-49烟碱样受体结合。 这诱导了JAK7 / STAT2 SOCS3信号通路的激活,有力地抑制了TNF-α的转录3。肾上腺的腹腔神经节还直接与产生乙酰胆碱的记忆T细胞亚群通讯,从而抑制了炎症性巨噬细胞47。
不变的自然杀伤性T细胞(iNKT)是识别CD1d而非肽抗原的微生物脂质的T细胞的专门子集。 NKT细胞是参与感染性病原体战斗和全身免疫调节的关键淋巴细胞群。 NKT细胞主要通过脾脏和肝脏的脉管系统和正弦波进行驻留和运输。 肝脏中的交感性β-肾上腺神经直接发出信号来调节NKT细胞的活性50。例如,在中风小鼠模型(MCAO)中,肝脏NKT细胞的活动性明显受到抑制,而交感神经或β-肾上腺素拮抗剂则逆转了这种情况。 此外,去甲肾上腺素能神经元对NKT细胞的这种免疫抑制活性导致全身感染和肺损伤增加。 因此,来自自主神经元的传出信号可以介导有效的免疫抑制。

Alex Jimenez博士的见解
神经源性炎症是由神经系统产生的局部炎症反应。 据信在多种健康问题的发病机理中起着基本作用,包括偏头痛,牛皮癣,哮喘,纤维肌痛,湿疹,酒渣鼻,肌张力障碍和多种化学敏感性。 尽管已经广泛研究了与周围神经系统相关的神经源性炎症,但是中枢神经系统内神经源性炎症的概念仍需要进一步研究。 然而,根据一些研究,镁缺乏被认为是神经源性炎症的主要原因。 下面的文章演示了神经系统中神经性炎症机制的概述,这可以帮助医疗保健专业人员确定最佳的治疗方法,以护理与神经系统相关的各种健康问题。
结论
体感和自主神经系统在调节炎症和免疫系统方面分别有哪些具体作用(图4)? 伤害感受器的激活导致局部轴突反射,其局部募集并激活免疫细胞,因此主要是促炎性的并且在空间上受到限制。 相反,自主神经刺激通过影响肝脏和脾脏中免疫细胞库而导致全身性免疫抑制。 人们对导致免疫抑制性迷走性胆碱能反射回路触发的周围传入信号机制知之甚少。 但是,迷走神经纤维中有80%到90%是初级传入感觉纤维,因此来自内脏的信号可能由脑干中的中间神经元激活,并通过它们传递到传入迷走纤维46的输出中,这些信号可能是免疫细胞驱动的。
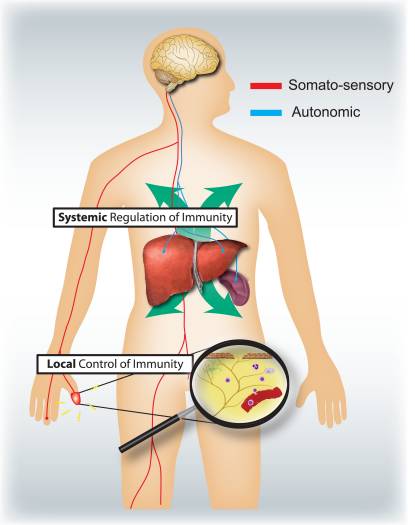
图4: 感觉和自主神经系统分别调节局部和全身免疫反应。 支配上皮表面(例如皮肤和肺)的伤害感受器诱导局部炎症反应,激活肥大细胞和树突状细胞。 在过敏性气道炎症,皮炎和类风湿关节炎中,伤害感受神经元在驱动炎症中起作用。 相比之下,支配内脏器官(例如脾脏和肝脏)的自主回路通过阻断巨噬细胞和NKT细胞活化来调节全身免疫反应。 在中风和败血性内毒素血症中,这些神经元起免疫抑制作用。
通常,炎症的时程和性质,无论是在感染,变态反应还是自身免疫病理过程中,都由所涉及的免疫细胞的种类来定义。 重要的是要知道哪些不同类型的免疫细胞受感觉和自主信号调节。 对伤害性感受器和自主神经元可以释放哪些介体的系统评估,以及不同的先天性和适应性免疫细胞对这些介体的受体表达,可能有助于解决这个问题。
在进化过程中,即使细胞具有完全不同的发育谱系,也已经为先天免疫和伤害感受开发了相似的危险检测分子途径。 尽管免疫学家和神经生物学家分别研究了PRR和有害的配体门控离子通道,但这两个领域之间的界线越来越模糊。 在组织损伤和病原体感染期间,危险信号的释放可能导致具有复杂双向通讯和整合宿主防御的周围神经元和免疫细胞的协同激活。 伤害感受器在与环境的界面上的解剖学定位,神经传导的速度及其释放免疫作用介体的有效混合物的能力使周围神经系统能够主动调节先天免疫反应并协调下游适应性免疫。 相反,伤害感受器对激活和敏化神经元的免疫介质高度敏感。 因此,神经源性和免疫介导的炎症不是独立的实体,而是一起充当预警装置。 但是,外周神经系统在许多免疫性疾病如哮喘,牛皮癣或结肠炎的病理生理学甚至病因学中也起着重要作用,因为其激活免疫系统的能力可以放大病理性炎症15-17。 因此,免疫疾病的治疗可能需要包括伤害感受器以及免疫细胞的靶向治疗。
致谢
我们感谢NIH的支持(2R37NS039518)。
总之,``了解神经源性炎症在宿主防御和免疫病理学方面的作用对于确定针对各种神经系统健康问题的正确治疗方法至关重要。 通过观察周围神经元与免疫细胞的相互作用,医护人员可以改进治疗方法,以进一步帮助增强宿主防御能力并抑制免疫病理学。 以上文章的目的是帮助患者了解神经病的临床神经生理学以及其他神经损伤健康问题。 国家生物技术信息中心(NCBI)引用的信息。 我们的信息范围仅限于脊椎治疗以及脊柱损伤和状况。 要讨论主题,请随时询问Jimenez博士或通过以下方式与我们联系。915-850-0900 。
由Alex Jimenez博士策划
附加主题:腰痛
背疼 是造成残障和世界各地缺勤时间最普遍的原因之一。 事实上,背痛被认为是第二次就诊最常见的原因,仅次于上呼吸道感染。 大约80%的人口在一生中至少会经历某种背痛。 脊柱是由骨骼,关节,韧带和肌肉以及其他软组织组成的复杂结构。 因此,受伤和/或病情加重,例如 椎间盘突出,最终会导致背部疼痛的症状。 运动伤害或汽车事故伤害通常是造成背痛的最常见原因,但是,有时最简单的动作可能会产生痛苦的结果。 幸运的是,诸如脊椎治疗等替代疗法可以通过使用脊柱调节和手动操作来帮助缓解背部疼痛,最终改善疼痛缓解。

特别重要的主题:腰痛管理
更多主题:额外:慢性疼痛和治疗
空白
参考资料
封闭手风琴
本文中关于“神经源性炎症的作用” 无意取代与合格的医疗保健专业人员或执业医师的一对一关系,也不是医疗建议。我们鼓励您根据您的研究以及与合格的医疗保健专业人员的合作关系做出医疗保健决策。
我们的信息范围 仅限于脊椎按摩疗法、肌肉骨骼、物理药物、健康、病因 内脏障碍 在临床表现、相关的躯体内脏反射临床动力学、半脱位复合体、敏感的健康问题和/或功能医学文章、主题和讨论中。
我们提供并呈现 临床合作 与来自不同学科的专家。 每位专家均受其专业执业范围和许可管辖范围的约束。 我们使用功能性健康和保健方案来治疗和支持肌肉骨骼系统损伤或疾病的护理。
我们的视频、帖子、主题、主题和见解涵盖与我们的临床实践范围相关并直接或间接支持我们的临床事务、问题和主题。*
我们的办公室已合理尝试提供支持性引文,并已确定支持我们帖子的相关研究或研究。 我们应要求向监管委员会和公众提供支持研究的副本。
我们了解我们承保的事项需要额外解释它如何有助于特定护理计划或治疗方案; 因此,要进一步讨论上述主题,请随时询问 亚历克斯·希门尼斯博士,哥伦比亚特区, 或与我们联系 915-850-0900.
我们在这里为您和您的家人提供帮助。
祝福
Alex Jimenez博士 直流电 麻省理工学院, 注册护士*, 科技委, 国际气候变化联合会*, 国际金融中心*, ATN*
电子邮件: Coach@elpasofunctionalmedicine.com
获得脊椎按摩疗法医生 (DC) 执照 德州 & 新墨西哥*
德克萨斯州特区许可证# TX5807,新墨西哥州 DC 许可证# NM-DC2182
获得注册护士 (RN*) 执照 in 佛罗里达
佛罗里达州执照 注册护士执照 # RN9617241 (控制编号 3558029)
紧凑状态: 多州许可证: 授权执业于 40个州*
Alex Jimenez 博士 DC、MSACP、RN* CIFM*、IFMCP*、ATN*、CCST
我的数字名片