我们小时候都被教导有五种感官:视觉、味觉、听觉、嗅觉和触觉。 最初的四种感官使用清晰、独特的器官,如眼睛、味蕾、耳朵和鼻子,但身体的感觉究竟是如何触摸的呢? 触摸是在整个身体上体验到的,包括内部和外部。 没有一个独特的器官负责感知触摸。 相反,整个身体周围都有微小的感受器或神经末梢,它们可以感知触摸发生的位置,并向大脑发送有关所发生触摸类型的信息的信号。 当舌头上的味蕾检测味道时,机械感受器是皮肤内和其他器官上检测触觉的腺体。 他们被称为 机械感受器 因为它们旨在检测机械感觉或压力差异。
机械感受器的作用
一个人明白,一旦负责发现特定感觉的器官向大脑发送信息,他们就会体验到感觉,大脑是处理和安排所有信息的主要器官。 信息通过称为神经元的导线从身体的所有区域发送到大脑。 有数以千计的小神经元分支到人体的所有区域,其中许多神经元的末端是机械感受器。 为了演示当您触摸物体时会发生什么,我们将使用一个示例。
想象一只蚊子落在你的手臂上。 这种昆虫的张力非常轻,刺激了手臂特定区域的机械感受器。 这些机械感受器沿着它们连接的神经元发送信息。 神经元一直连接到大脑,大脑在发送信息的特定机械感受器的确切位置接收到某物正在接触你的身体的信息。 大脑会按照这个建议行事。 也许它会告诉眼睛查看检测到签名的手臂区域。 当眼睛告诉大脑手臂上有一只蚊子时,大脑可能会告诉手迅速将它弹开。 这就是机械感受器的工作原理。 下面这篇文章的目的是展示和详细讨论机械感受器的功能组织和分子决定因素。
触觉:机械敏感受体的功能组织和分子决定因素
抽象
皮肤机械感受器位于皮肤的各个层,在那里它们检测到广泛的机械刺激,包括光刷、拉伸、振动和有害压力。 这种不同的刺激与各种专门的机械感受器相匹配,这些感受器以特定的方式对皮肤变形做出反应,并将这些刺激传递给更高的大脑结构。 对机械感受器和基因易处理的感觉神经末梢的研究开始揭示触觉机制。 该领域的工作使研究人员对触觉感知背后的电路组织有了更透彻的了解。 新型离子通道已成为转导分子的候选者,机械门控电流的特性提高了我们对触觉刺激适应机制的理解。 这篇综述重点介绍了在多毛和无毛皮肤中机械感受器的功能特性以及检测机械输入和形状机械感受器适应的离子通道方面取得的进展。
关键词: 机械感受器, 机械敏感通道, 疼痛, 皮肤, 体感系统, 触摸
介绍
触摸是检测影响皮肤的机械刺激,包括无害和有害的机械刺激。 它是哺乳动物和人类生存和发展的重要意义。 固体物体和液体与皮肤的接触为中枢神经系统提供了必要的信息,从而允许探索和识别环境并启动运动或有计划的手部运动。 触摸对于学徒、社交和性行为也非常重要。 触觉是最不脆弱的感觉,尽管在许多病理情况下它可能会被扭曲(感觉过敏、感觉迟钝)。1-3
触摸响应涉及非常精确的机械信息编码。 皮肤机械感受器位于皮肤的各个层,在那里它们可以检测到广泛的机械刺激,包括轻刷、拉伸、振动、头发偏转和有害压力。 这种不同的刺激与各种专门的机械感受器相匹配,这些感受器以特定的方式对皮肤变形做出反应,并将这些刺激传递给更高的大脑结构。 皮肤的体感神经元分为两组:对良性压力作出反应的低阈值机械感受器 (LTMR) 和对有害机械刺激作出反应的高阈值机械感受器 (HTMR)。 LTMR 和 HTMR 细胞体位于背根神经节 (DRG) 和颅感觉神经节 (三叉神经节) 内。 与 LTMR 和 HTMR 相关的神经纤维根据其动作电位传导速度分为 Aβ-、Aβ-或 C-纤维。 C 纤维无髓鞘,传导速度最慢(~2 m/s),而 A? 和A? 纤维有轻度和重度有髓鞘,分别表现出中等 (~12 m/s) 和快速 (~20 m/s) 传导速度。 LTMR 也根据其对持续机械刺激的适应率分为缓慢或快速适应反应(SA-和 RA-LTMR)。 它们的特征还在于它们所支配的皮肤终末器官和它们所偏好的刺激。
机械感受器检测机械信号的能力依赖于机械传感器离子通道的存在,该离子通道可将机械力迅速转化为电信号并使感受野去极化。 这种称为受体电位的局部去极化可以产生向中枢神经系统传播的动作电位。 然而,介导机械转导和适应机械力的分子的特性仍不清楚。
在这篇综述中,我们概述了哺乳动物机械感受器在多毛和无毛皮肤中无害和有害触摸的特性。 我们还考虑了最近关于机械门控电流特性的知识,试图解释机械感受器适应的机制。 最后,我们回顾了在识别负责产生机械门控电流的离子通道和相关蛋白质方面取得的最新进展。
无害的触摸
毛囊相关的 LTMR
毛囊代表产生毛干的微型器官,可检测轻触。 与毛囊相关的纤维通过在刺激开始和消除时触发动作电位序列来响应毛发运动及其方向。 它们正在迅速适应受体。
猫和兔子。 在猫和兔毛中,毛囊可分为三种毛囊类型,即羽绒毛、卫毛和Tylotrichs。 绒毛(绒毛、羊毛、毳毛)4 是被毛中数量最多、最短和最细的毛发。 它们呈波浪状,无色,从皮肤的一个共同孔口以两到四根毛发为一组出现。 卫毛(单头毛、耳毛、顶毛)4 略微弯曲,有色素或无色素,从毛囊口单独长出。 tylotrichs 是数量最少、最长和最厚的毛发。5,6 它们有色素或无色素,有时两者兼而有之,并且单独从被毛细血管环包围的毛囊中出现。 供给毛囊的感觉纤维位于皮脂腺下方,属于 A? 或 A?-LTMR 纤维。 7
紧邻下毛干,皮脂腺水平下方是披针形毛-鲁菲尼末端环。 这些感觉神经末梢位于形成毛囊的结缔组织内围绕毛干的螺旋路线。 在毛囊内,也有游离的神经末梢,其中一些形成机械感受器。 通常,触球(见无毛皮肤)围绕在tylotrich 滤泡的颈部区域。
在 1930 年至 1970 年期间,人们对猫和兔毛皮中的有髓神经末梢的特性进行了深入研究(Hamann 的评论,1995 年)8。值得注意的是,Brown 和 Iggo 研究了来自猫的隐神经中的 772 个单位的有髓传入神经纤维和兔子,将反应分为三种受体类型,对应于羽绒毛(D 型受体)、卫毛(G 型受体)和 Tylotrich 毛(T 型受体)的运动。 9 所有的传入神经纤维反应都汇集在一起通过对抗名为 RA II 的 Pacinian 受体,在 I 型快速适应受体 (RA I) 中发挥作用。 RA I 机械感受器检测机械刺激的速度并具有锐利的边界。 它们不检测热变化。 伯吉斯等人。 还描述了一种快速适应的场感受器,它对皮肤的抚摸或几根毛发的运动做出最佳反应,这归因于对 pilo-Ruffini 末端的刺激。 毛囊反应没有一个归因于 C 纤维活性。 10
老鼠。 在小鼠的背部毛状皮肤中,已经描述了三种主要类型的毛囊:锯齿形(约 72%)、锥子/欧氏(约 23%)和卫毛或 tylotrich(约 5%)。11-14 之字形和锥子/ auchenne 毛囊产生更细和更短的毛干,并与一个皮脂腺有关。 Guard 或 tylotrich 毛发是毛囊类型中最长的。 它们的特征是与两个皮脂腺相关的大毛球。 卫毛和锥子/欧歇内毛以迭代的、规则间隔的模式排列,而锯齿状毛密集地分布在两个较大毛囊类型周围的皮肤区域 [图。 1(A1、A2 和 A3)]。
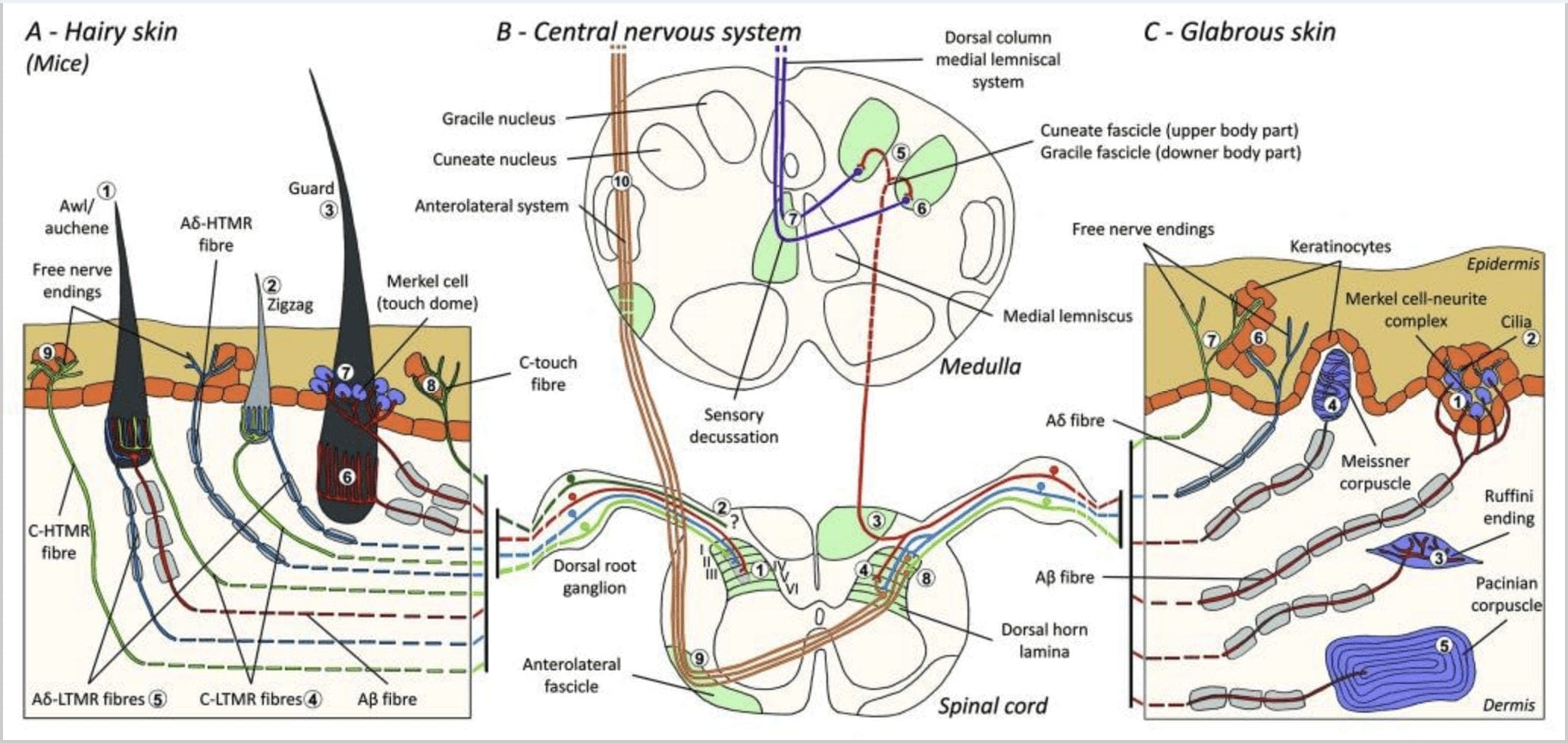
图1。 皮肤机械感受器的组织和投射。 在有毛的皮肤中,轻刷和触摸主要通过毛囊周围的神经支配来检测:锥/欧兴 (A1)、锯齿形 (A2) 和防护 (A3)。 C-LTMR 披针形末端 (A4)、A?-LTMR 和 A? 快速适应-LTMR (A6)。 之字形毛囊是较短的毛干,受 C-LTMR (A4) 和 A? -LTMR 披针形尾端 (A5)。 最长的保护毛囊受 A? 快速适应-LTMR 纵向披针形末端 (A6) 并与 A? 触摸圆顶末端的缓慢适应-LTMR (A7)。 所有这些纤维的中心突出部分终止于脊髓背角的不同但部分重叠的椎板(C-LTMR 在椎板 II 中,Aβ-LTMR 在椎板 III 中,Aβ-LTMR 在椎板 IV 和 V 中)。 支配相同或相邻毛囊的 LTMR 的突起排列成脊髓背角中的窄柱(B1 为灰色)。 只有在有毛的皮肤中,C 纤维游离末端的亚群才会支配表皮并对愉悦的触感做出反应 (A8)。 这些 C-touch 纤维不会对有害触摸做出反应,并且它们的路径路径尚不清楚 (B2)。 在无毛皮肤中,无害的触摸由四种类型的 LTMR 介导。 Merkel 细胞-神经突复合体位于表皮的基底层 (C1)。 这种机械感受器由许多默克尔细胞之间的排列和来自单个 A? 的扩大的神经末梢组成。 纤维。 Merkel 细胞表现出接触角质形成细胞 (C2) 的手指状突起。 Ruffini 末端位于真皮中。 它是一个薄薄的雪茄形封装的感觉末端,连接到 A? 纤维(C3)。 与 A 相连的迈斯纳小体? 神经末梢位于真皮乳头。 这种封装的机械感受器由堆积的支持细胞组成,这些细胞排列为被结缔组织 (C4) 包围的水平薄片。 帕西尼亚小体是较深的机械感受器。 一个单A? 无髓神经末梢终止于这个由同心薄片组成的大卵形小体的中心。 这些 Aβ-LTMR 纤维在脊髓中的投射分为两个分支。 主要中央分支 (B3) 在脊髓同侧背侧上升,在初级传入神经形成其第一个突触 (B5) 的髓质水平上形成楔形或细束 (B6)。 次级神经元进行感觉交叉(B7)以在内侧丘系上形成一条通道,该通道通过脑干上升到中脑,特别是在丘脑中。 LTMR 的次级分支终止于椎板 II、IV、V 的背角并干扰疼痛传递 (B4)。 有毛 (A9) 和无毛皮肤 (C7) 的表皮中的游离神经末梢可以检测到有害的触摸。 这些机械感受器是 Aβ-HTMR 和 C-HTMR 与相邻角质形成细胞 (C6) 紧密接触的末端。 A?-hTMR 终止于椎板 I 和 V; C-HTMR 终止于椎板 I 和 II (B8)。 在脊髓背角水平,初级传入 HTMR 与次级神经元形成突触,这些神经元穿过中线并爬到前外侧束中的更高大脑结构 (B9, B10)。
最近,Ginty 和合作者结合使用分子遗传标记和体细胞逆行追踪方法来可视化小鼠 LTMR 的外周和中央轴突末端的组织。 15 他们的发现支持一个模型,其中复杂触觉刺激的个体特征是由三种毛囊类型提取,并通过 A?-、A?- 和 C- 纤维的独特组合的活动传送到背角。
他们表明,酪氨酸羟化酶阳性 (TH+) DRG 神经元的基因标记表征了一群非肽能、小直径感觉神经元,并允许在皮肤中显示 C-LTMR 外周末梢。 令人惊讶的是,发现单个 C-LTMR 的轴突分支呈树枝状并形成纵向披针形末端,这些末端与锯齿形(80% 的末端)和锥子/欧歇(20% 的末端)密切相关,但与 tylotrich 毛囊无关 [图。 1 (A4)]。 纵向披针形末端一直被认为只属于 A?-LTMR,因此 C-LTMR 的末端会形成纵向披针形末端是出乎意料的。 15 这些 C-LTMR 与缓慢和快速适应相比具有中间适应有髓机械感受器 [图。 2 (C1)]。
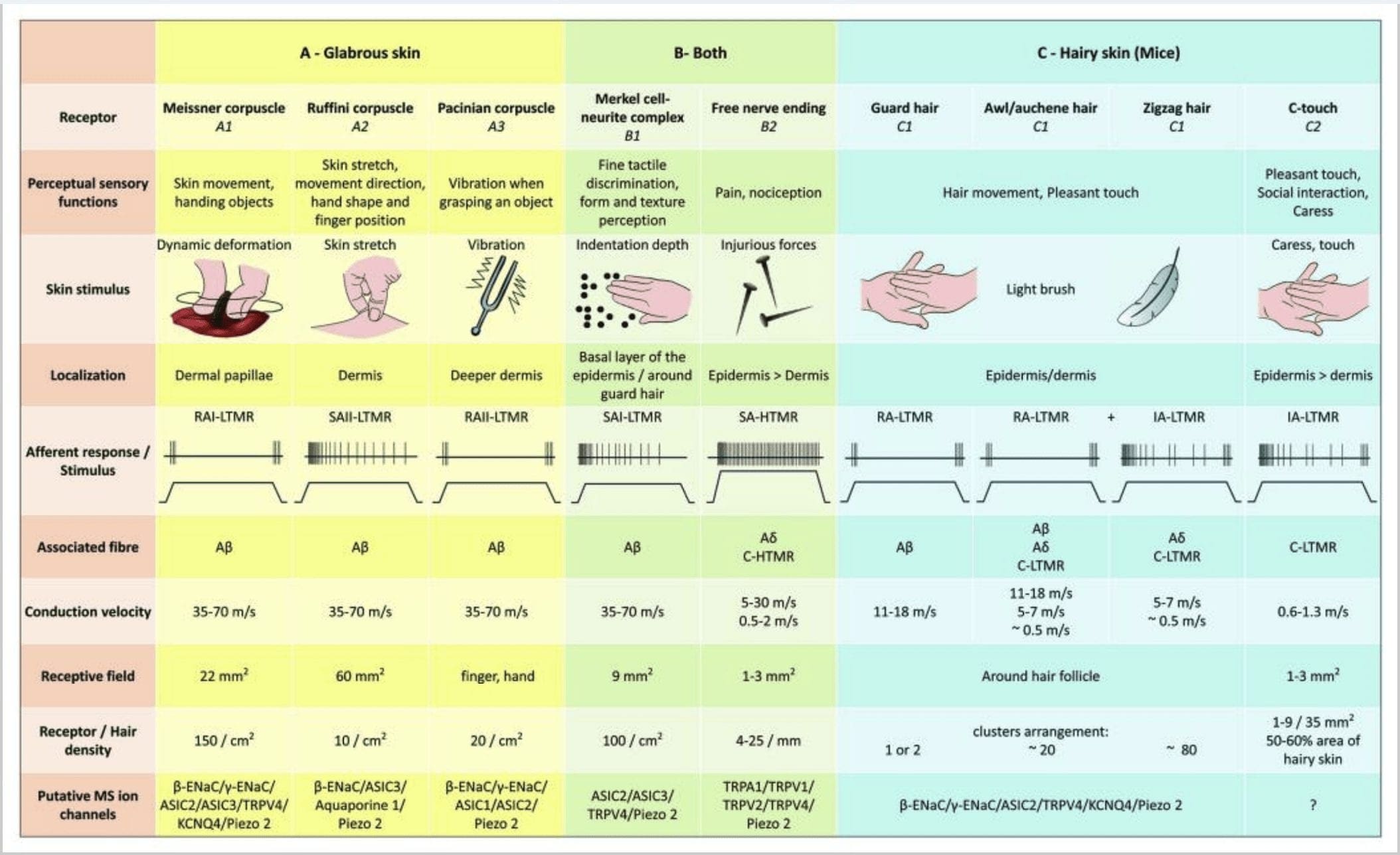
图2。 哺乳动物的触觉感受器:皮肤触觉感受器分化为由多个感受器支持的无害触觉,在无毛和多毛的皮肤中具有低机械阈值 (LTMR) 和由高机械阈值受体 (HTMR) 支持的有害触觉。 它们构成主要终止于表皮的神经游离末梢。 (A) 无毛的皮肤。 A1:迈斯纳小体检测皮肤运动和手中物体的滑动。 它们对于处理物体和灵巧很重要。 受体迅速适应刺激,与 A? 纤维和稀疏到 C 纤维,并有大的受体场。 A2:Ruffini 小体检测皮肤拉伸,对于检测手指位置和处理对象很重要。 只要施加刺激,受体就会慢慢适应刺激并保持活动。 受体连接到 A? 纤维并具有较大的感受野。 A3:Pacinian 小体位于真皮深处,可检测振动。 受体连接到 A? 纤维; 他们迅速适应刺激并拥有最大的感受野。 (B) 整个皮肤。 B1:默克尔细胞复合物存在于无毛的皮肤和头发周围。 它们在手中密集表达,对于纹理感知和两点之间的最佳区分很重要。 他们负责手指精度。 受体连接到 A? 纤维; 他们慢慢适应刺激,感受野较短。 B2:对刺激适应非常缓慢的有害触摸 HTMR,即只要施加伤害性刺激就会活跃。 它们是由 A? 的游离神经末梢形成的。 和与角质形成细胞相关的 C 纤维。 (C) 毛茸茸的皮肤。 C1:毛囊与不同的头发类型有关。 在小鼠中,卫毛是较长且稀疏的一种,锥子/欧兴毛是中等大小的,而锯齿形是最小和最密集的毛发。 它们连接到 A? 纤维还要A? 和 C-LTMRs 纤维,用于锥子/欧歇纳和锯齿形头发。 它们检测毛发运动,包括在爱抚过程中的愉悦触感。 他们迅速或以中等动力学适应刺激。 C2:C-touch 神经末梢对应于 C 纤维末端的亚型,具有以低机械阈值为特征的自由末端。 它们应该编码由爱抚引起的愉悦感。 他们适度地适应刺激并且具有短的感受野。 不同触觉受体中表达的假定机械敏感 (MS) 离子通道根据初步数据显示,并总结评估中的当前假设。
确定的第二个主要人群涉及 Awl/Auchenne 和之字形毛囊中的 A?-LTMR 末端,以与猫和兔子中广泛研究的羽绒毛囊进行比较。 Ginty 和合作者表明,TrkB 在中等直径 DRG 神经元的一个子集中高水平表达。 使用标记纤维的离体皮肤神经制剂进行的细胞内记录显示,它们表现出先前在猫和兔身上研究过的纤维的生理特性:出色的机械敏感性(Von Frey 阈值 < 0.07 mN)、对超阈值刺激的快速适应反应、中间传导速度(5.8 × 0.9 m/s)和狭窄的未弯曲的胞体尖峰。15 这些 A?-LTMR 形成纵向披针形末端,与躯干的几乎每个锯齿形和锥子/欧歇毛囊相关 [图。 1 (A5)]。
最后,他们证明了快速适应 A? LTMRs 形成与保护(或 tylotrich)和锥/欧歇毛囊相关的纵向披针形末端 [图。 1 (A6)].15 此外,保护毛还与默克尔细胞复合体相关,形成与 A 相连的触摸圆顶? 慢慢适应 LTMR [图。 1 (A7)]。
总之,几乎所有锯齿形毛囊都受到 C-LTMR 和 A?-LTMR 披针形末端的神经支配。 锥子/欧歇内毛发受 A 的三重神经支配? 快速适应-LTMR、A?-LTMR和C-LTMR披针形末端; 保护毛囊受 A? 快速适应-LTMR 纵向披针形末端并与 A? 慢慢适应触摸圆顶末端的 LTMR。 因此,每个小鼠毛囊都会收到与神经生理学上不同的机械感觉末端器官相对应的 LTMR 末端的独特且不变的组合。 考虑到这三种头发类型的迭代排列,Ginty 和合作者提出毛状皮肤由外围单元的迭代重复组成,包括:(1) 一根或两根位于中心的护毛,(2) 约 20 根周围的锥子/欧兴毛和 (3 ) ~80 根散布的锯齿状毛发 [图。 2 (C1)]。
脊髓投射。 A的中心投影? 快速适应-LTMRs、Aβ-LTMRs 和 C-LTMRs 在脊髓背角的不同但部分重叠的椎板(II、III、IV)中终止。 此外,支配外周 LTMR 单元内相同或相邻毛囊的 LTMR 的中央末端对齐以在脊髓背角形成狭窄的 LTMR 柱 [图。 1 (B1)]。 因此,似乎背角中的一个楔形或一列躯体组织的初级感觉传入末端代表了 A?-、A?-和 C-LTMR 的中央投影的排列,它们支配着相同的外围单元并检测机械刺激作用于同一小群毛囊。 根据躯干和四肢的卫毛、锥毛/奥金毛和锯齿形毛的数量以及每个 LTMR 亚型的数量,Ginty 和合作者估计小鼠背角包含 2,000 到 4,000 根 LTMR 柱,这对应于外周毛的大致数量LTMR 单位.15
此外,LTMR 亚型的轴突彼此密切相关,具有缠绕的突起和交错的披针形末端,支配同一毛囊。 此外,由于三种毛囊类型表现出不同的形状、大小和细胞组成,它们可能具有不同的偏转或振动调谐特性。 这些发现与猫和兔子的经典神经生理学测量结果一致,表明 A? RA-LTMRs 和 A?-LTMRs 可以通过不同毛囊类型的偏转而被不同地激活。 16,17
总之,多毛皮肤的触感是:(1)三种毛囊的相对数量、独特的空间分布以及不同的形态和偏转特性; (2) 与三种毛囊类型中的每一种相关的 LTMR 亚型末端的独特组合; (3) 毛囊相关 LTMR 的四种主要类别的不同敏感性、传导速度、脉冲序列模式和适应特性,使多毛皮肤机械感觉系统能够提取和传达定义为中枢神经系统的复杂质量组合触碰。
自由神经末梢 LTMR
通常,皮肤中的 C 纤维游离末端是 HTMR,但 C 纤维的一个亚群对有害触摸没有反应。 这个触觉 C 纤维 (CT) 传入子集代表了一种独特类型的无髓、低阈值机械感受单元,存在于人类和哺乳动物的多毛但不无毛的皮肤中 [图。 1 (A8)].18,19 CT 通常与身体接触中愉快的触觉刺激的感知有关。20,21
CT 传入神经对 0.3 到 2.5 mN 范围内的压痕力有反应,因此与许多 A? afferents.19 因此,CT 传入神经的适应特征与适应缓慢和快速适应的有髓机械感受器相比处于中等水平。 人类 CT 传入神经的感受野大致呈圆形或椭圆形。 该区域由 35 到 2.22 个小响应点组成,分布在最大 50 mm60 的区域中。2 小鼠同源受体以不连续斑块的形式组织起来,覆盖毛皮中约 2-23% 的区域 [图。 XNUMX (CXNUMX)].XNUMX
来自缺乏有髓触觉传入的患者的证据表明,CT 纤维中的信号激活了岛叶皮质。 由于该系统在对触觉的辨别方面进行编码方面很差,但非常适合对缓慢、轻柔的触觉进行编码,因此多毛皮肤中的 CT 纤维可能是处理触觉的愉悦和社会相关方面的系统的一部分。 24 CT 纤维激活也可能具有抑制疼痛的作用,最近有人提出炎症或创伤可能会将 C 纤维 LTMR 传递的感觉从愉快的触摸转变为疼痛。 25,26
CT 传入的路径尚不清楚 [图。 1 (B2)],但已记录到脊髓丘脑投射细胞的低阈值触觉输入,27 证明了在脊索切开手术后这些通路被破坏后,人类患者对侧触觉检测的微妙缺陷的报道。 28
无毛皮肤中的 LTMR
默克尔细胞-神经突复合物和触摸圆顶。 Merkel (1875) 是第一个对具有大的分叶状核的表皮细胞簇进行组织学描述,这些细胞与假定的传入神经纤维接触。 他假设他们通过称他们为 Tastzellen(触觉细胞)来降低触觉。 在人类中,默克尔细胞神经突复合物富含于皮肤的触敏区域,它们存在于手指、嘴唇和生殖器的表皮基底层中。 它们也以较低的密度存在于有毛的皮肤中。 默克尔细胞神经突复合体由一个默克尔细胞组成,该细胞与单个有髓 A? 纤维[图。 1 (C1)](Halata 和合作者的评论)。29 在表皮侧,默克尔细胞表现出在相邻角质形成细胞之间延伸的手指状突起 [图。 1 (C2)]。 Merkel 细胞是角质形成细胞衍生的表皮细胞。30,31 引入了 touch dome 一词来命名猫前爪毛茸茸的皮肤中大量集中的 Merkel 细胞复合物。 一个触摸圆顶可能有多达 150 个默克尔细胞,由单个 A?-纤维和在人类中除 A?-纤维、A? 和 C 纤维也经常存在。 32-34
刺激 Merkel 细胞神经突复合物会导致缓慢适应的 I 型 (SA I) 反应,其起源于具有尖锐边界的点状感受野。 没有自发放电。 这些复合物对皮肤的压痕深度有反应,并具有皮肤机械感受器的最高空间分辨率 (0.5 mm)。 它们传输触觉刺激的精确空间图像,并被提议负责形状和纹理辨别[图。 2 (B1)]。 没有默克尔细胞的小鼠无法用脚检测纹理表面,而用胡须检测。35
默克尔细胞、感觉神经元还是两者都是机械转导的位点仍然存在争议。 在大鼠中,Merkel 细胞的光毒性破坏消除了 SA I 反应。 36 在具有基因抑制的 Merkel 细胞的小鼠中,在离体皮肤/神经制剂中记录的 SA I 反应完全消失,这表明默克尔细胞是正确编码默克尔所必需的受体反应。37 然而,通过电机驱动压力对培养中的分离的默克尔细胞进行机械刺激不会产生机械门控电流。38,39 角质形成细胞可能在默克尔细胞神经突复合物的正常功能中发挥重要作用。 默克尔细胞指状突起可以随着皮肤变形和表皮细胞运动而运动,这可能是机械转导的第一步。 显然,研究默克尔细胞的机械敏感性所需的条件尚未建立。
鲁菲尼结局。 Ruffini 结尾是与 A? 神经末梢。 Ruffini 末端是沿着真皮胶原蛋白链排列的小结缔组织圆柱体,由 4 到 6 根直径为 1 3 微米的有髓神经纤维提供。 真皮中多达三个不同方向的圆柱体可以合并形成一个受体[图。 2 (C2)]。 在结构上,鲁菲尼尾端类似于高尔基腱器官。 它们在真皮中广泛表达,并已被确定为缓慢适应的 II 型 (SA II) 皮肤机械感受器。 在自发神经活动的背景下,通过垂直低力保持机械刺激或更有效地通过皮肤拉伸引起缓慢适应的规律放电。 SA II 响应源自边界模糊的大感受野。 Ruffini 受体通过皮肤拉伸模式有助于感知物体运动的方向[图。 XNUMX (AXNUMX)]。
在小鼠中,SA I 和 SA II 反应可以在离体神经皮肤制备中进行电生理学分离。 40 Nandasena 和合作者报告了水通道蛋白 1 (AQP1) 在大鼠门牙牙周 Ruffini 末端的免疫定位,这表明 AQP1 参与维持机械传导所必需的牙齿渗透平衡。 41 牙周 Ruffini 末端也表达了推定的机械敏感离子通道 ASIC3.42
迈斯纳小体。 迈斯纳小体位于无毛皮肤的真皮乳头中,主要存在于手掌和足底,但也存在于嘴唇、舌头、面部、乳头和生殖器中。 从解剖学上讲,它们由一个封装的神经末梢组成,该胶囊由扁平的支持细胞组成,这些细胞排列成嵌入结缔组织中的水平薄片。 有一根神经纤维A? 每个小体连接的传入 [图。 1 (C4)]。 小体的任何物理变形都会触发一系列动作电位,这些动作电位很快就会停止,即它们正在迅速适应受体。 当刺激被移除时,红细胞恢复其形状,同时产生另一组动作电位。 由于它们在真皮中的浅表位置,这些小体选择性地响应皮肤运动、滑动和振动的触觉检测 (20-40 Hz)。 它们对动态皮肤很敏感——例如,在皮肤和正在处理的物体之间[图。 2 (A1)]。
帕西尼亚小体。 帕西尼亚小体是皮肤较深的机械感受器,是皮肤运动最敏感的有壳皮肤机械感受器。 这些由纤维结缔组织的同心薄片和由扁平修饰的雪旺细胞衬里的成纤维细胞组成的大卵形小体(长 1 毫米)在真皮深处表达。 43 在小体的中心,在称为内球的充满液体的空腔中, 终止一个单一的 A? 传入无髓神经末梢[图。 1 (C5)]。 它们在皮肤表面有一个大的感受野和一个特别敏感的中心。 在 c-Maf 突变小鼠中,几种快速适应的机械感受器类型的发育和功能被破坏。 尤其是 Pacinian 小体严重萎缩。 44
帕西尼亚小体对皮肤的压痕表现出非常快速的适应,即快速适应 II (RA II) 神经放电,能够跟随高频振动刺激,并允许通过传递的振动感知远处的事件。 45 帕西尼亚小体传入神经在刺激开始和抵消时对持续的压痕做出反应。 它们也被称为加速度检测器,因为它们可以检测刺激强度的变化,如果刺激的变化率发生变化(如振动中发生的那样),它们的响应就会与这种变化成比例。 Pacinian 小体感知总压力变化和大多数振动(150-300 Hz),它们甚至可以在几厘米远的地方检测到[图。 2 (A3)]。
在去壳的 Pacinian 小体中观察到强直反应。 46 此外,在持续的压痕刺激期间,完整的 Pacinian 小体以持续的活动响应,而当 GABA 介导的信号传导在板状胶质细胞和神经末梢之间被阻断时,不会改变机械阈值或响应频率。 47 因此, Pacinian 小体的非神经元成分可能在过滤机械刺激和调节感觉神经元的反应特性方面具有双重作用。
脊髓突起。 脊髓中 Aβ-LTMR 的投影分为两个分支。 主要的中央分支在同侧背柱的脊髓中上升到颈部水平[图。 1 (B3)]。 例如,次级分支终止于椎板 IV 的背角并干扰疼痛传递。 作为门控的一部分,这可能会减轻疼痛 [图。 1 (B4)].48
在颈部水平,主要分支的轴突分为两个束:中线束包括从身体下半部(腿和躯干)传递信息的短束束,外束包括从上半部传递信息的楔形束身体(手臂和躯干)[图。 1 (B5)]。
初级触觉传入神经在髓质中与二级神经元形成第一个突触,其中来自每个束的纤维在同名的核中突触:薄束轴突突触在细长核中,楔形轴突突触在楔形核中[图。 1 (B6)]。 接受突触的神经元提供次级传入神经并立即穿过中线,在脑干对侧形成一个束——内侧丘系——它通过脑干上升到中脑的下一个中继站,特别是丘脑[图. 1 (B7)]。
LTMR 的分子规格。 最近部分阐明了控制 LTMR 早期多样化的分子机制。 Bourane 和合作者已经证明,在 E2-11 胚胎小鼠 DRG 中表达 Ret 酪氨酸激酶受体 (Ret) 及其共同受体 GFR?13 的神经元群体选择性地共同表达转录因子 Mafa。49,50 这些作者证明了 Mafa/ Ret/GFR?2 神经元在出生时注定成为三种特定类型的 LTRM:支配默克尔细胞复合物的 SA1 神经元、支配迈斯纳小体的快速适应神经元和在毛囊周围形成披针形末端的快速适应传入神经 (RA I)。 Ginty 和合作者还报告说,表达 early-Ret 的背根神经节神经元正在迅速适应来自迈斯纳小体、帕西尼亚小体和毛囊周围披针形末端的机械感受器。 51 它们支配纤细和楔形核内的离散目标区域,揭示了一种特定于模式的机械感觉模式脑干内的神经元轴突投射。
探索人体皮肤机械感受器。 Hagbarth 和 Vallbo 在 1968 年描述的“微神经造影”技术已应用于研究提供肌肉、关节和皮肤的单个人体机械敏感末端的放电行为(参见 Macefield,2005 年的评论)。52,53 大多数人体皮肤微神经造影研究已经描述了手无毛皮肤中触觉传入的生理学特征。 来自人类受试者的正中神经和尺神经的微电极记录揭示了由四类 LTMR 产生的触觉:Meissner 传入神经对穿过皮肤的光抚特别敏感,对局部剪切力和感受野内的初始或明显滑动作出反应。 Pacinian 传入神经对轻快的机械瞬变非常敏感。 传入神经对吹过感受野的反应强烈。 位于手指中的 Pacinian 小体通常会对敲击支撑手臂的桌子做出反应。 Merkel 传入神经的特点是对施加到离散区域的压痕刺激具有高动态敏感性,并且通常在释放期间以关闭放电作出反应。 尽管 Ruffini 传入神经对正常施加在皮肤上的力有反应,但 SA II 传入神经的一个独特特征是它们也能对横向皮肤拉伸作出反应。 最后,前臂的毛发单位具有大的卵形或不规则的感受野,由多个敏感点组成,这些敏感点对应于单个毛发(每个传入供应约 20 根毛发)。
角质形成细胞的机械敏感性
皮肤上的任何机械刺激都必须通过形成表皮的角质形成细胞传递。 除了它们的支持或保护作用之外,这些无处不在的细胞还可以执行信号传导功能。 例如,角质形成细胞分泌 ATP,一种重要的感觉信号分子,以响应机械和渗透性刺激。 54,55 ATP 的释放通过嘌呤能受体的自分泌刺激诱导细胞内钙增加。 55 此外,有证据表明低渗性激活 Rho -激酶信号通路和随后的F-肌动蛋白应力纤维形成表明角质形成细胞的机械变形可能会机械干扰邻近细胞,例如用于无害触摸的默克尔细胞和用于有害触摸的C-纤维游离末端[图。 1 (C6)].56,57
有害之触
高阈值机械感受器 (HTMR) 是表皮 C- 和 A? 游离神经末梢。 它们与特殊结构无关,并且在多毛皮肤中都可以观察到[图。 1(A9)]和无毛皮肤[图。 1(C7)]。 然而,必须谨慎考虑游离神经末梢的术语,因为神经末梢总是与角质形成细胞或朗格朗斯细胞或黑素细胞紧密并列。 神经末梢的超微结构分析显示存在粗面内质网、丰富的线粒体和致密的核心囊泡。 表皮细胞的相邻膜增厚,类似于神经组织中的突触后膜。 请注意,神经末梢和表皮细胞之间的相互作用可能是双向的,因为表皮细胞可能会释放介质,如 ATP、白介素(IL6、IL10)和缓激肽,相反,肽能神经末梢可能会释放作用于表皮细胞的肽,如 CGRP 或 P 物质。 HTMR 包含仅由有害机械刺激和多模式伤害感受器激发的机械伤害感受器,这些伤害感受器也对有害热量和外源性化学物质有反应 [图。 2 (B2)].58
HTMR 传入纤维终止于脊髓背角的投射神经元。 Aβ-HTMRs 主要在 I 层和 V 层中接触二级神经元,而 C-HTMRs 在层 II 中终止[图。 1 (B8)]。 二级伤害性神经元投射到脊髓的控制侧并在白质中上行,形成前外侧系统。 这些神经元主要终止于丘脑[图。 1(B9 和 B10)]。
体感神经元中的机械电流
机械感受器缓慢或快速适应的机制尚未阐明。 目前尚不清楚感觉神经末梢的细胞环境、机械门控通道的内在特性和感觉神经元中轴突电压门控离子通道的特性在多大程度上提供了机械感受器适应(图 2)。 然而,机械门控电流表征的最新进展表明,DRG 神经元中存在不同类别的机械敏感通道,并且可以解释机械感受器适应的某些方面。
啮齿动物的体外记录表明,DRG 神经元的胞体本质上是机械敏感的,并表达阳离子机械门控电流。 59-64 钆和钌红完全阻断机械敏感电流,而在生理浓度下,外部钙和镁以及阿米洛利和苯扎米,导致部分阻滞。 60,62,63 FM1-43 作为持久阻滞剂,将 FM1-43 注射到小鼠后爪可降低 Randall�Selitto 测试中的疼痛敏感性并增加评估的缩爪阈值与冯弗雷头发.65
响应持续的机械刺激,机械敏感电流通过闭合而下降。 基于电流衰减的时间常数,区分了四种不同类型的机械敏感电流:快速适应电流(~3-6 ms)、中等适应电流(~15-30 ms)、缓慢适应电流(~200-300 ms) ) 和超慢适应电流 (~1000 ms)。64 所有这些电流在支配后爪无毛皮肤的大鼠 DRG 神经元中以不同的发生率存在。64
机械敏感电流的机械敏感性可以通过应用一系列增量机械刺激来确定,从而可以进行相对详细的刺激-电流分析。 66 刺激-电流关系通常是 S 型的,电流的最大幅度由同时打开的通道。 64,67 有趣的是,据报道,与超慢适应的机械敏感电流相比,快速适应的机械敏感电流显示出较低的机械阈值和半激活中点。 63,65
具有非伤害性表型的感觉神经元优先表达具有较低机械阈值的快速适应机械敏感电流。 60,61,63,64,68 相反,在假定的非伤害性细胞中偶尔报道缓慢和超慢适应机械敏感电流。 64,68这提示了这些电流可能有助于在体内 LTMR 和 HTMR 中看到的不同机械阈值。 尽管这些体外实验应谨慎进行,但对培养的小鼠感觉神经元的径向拉伸刺激也提供了对 DRG 神经元体细胞中存在低阈值和高阈值机械传感器的支持。 69 该范例揭示了两个拉伸敏感神经元的主要群体,一种对低刺激幅度有反应,另一种对高刺激幅度有选择性反应。
这些结果具有重要但推测性的机械含义:感觉神经元的机械阈值可能与机械感受器的细胞组织几乎没有关系,但可能在于机械门控离子通道的特性。
最近揭示了大鼠 DRG 神经元中机械敏感性阳离子电流脱敏的机制。64,67 它是由影响通道特性的两种并发机制引起的:适应和失活。 适应最初是在听觉毛细胞研究中报道的。 它在操作上可以描述为传感器通道的激活曲线沿机械刺激轴的简单平移。70-72 适应允许感觉受体在存在现有刺激的情况下保持其对新刺激的敏感性。 然而,在调节机械刺激后,DRG 神经元中的大部分机械敏感电流无法重新激活,这表明某些传感器通道失活。64,67 因此,失活和适应协同作用以调节机械敏感电流。 这两种机制对大鼠 DRG 神经元中鉴定的所有机械敏感电流都是共同的,这表明相关的物理化学元素决定了这些通道的动力学。 64
总之,在体外确定内源性机械敏感电流的特性对于在分子水平上识别转导机制至关重要。 在 DRG 神经元中观察到的机械阈值和不同机械门控电流的适应动力学的变化表明,离子通道的内在特性可以至少部分解释 1960 年描述的机械感受器的机械阈值和适应动力学。 80 使用离体制剂。
推定的机械敏感蛋白
体感神经元中的机械敏感离子电流具有很好的特征,相比之下,对于哺乳动物中介导机械转导的分子的身份知之甚少。 果蝇和秀丽隐杆线虫的遗传筛选已经确定了候选机械转导分子,包括 TRP 和退化素/上皮钠离子通道 (Deg/ENaC) 家族。 73 最近试图阐明哺乳动物机械转导分子基础的尝试主要集中在这些候选分子的同源物上. 此外,许多这些候选物存在于皮肤机械感受器和体感神经元中(图 2)。
酸感应离子通道
ASIC 属于退化-上皮 Na+ 通道家族的质子门控亚组。74 ASIC 家族的三个成员(ASIC1、ASIC2 和 ASIC3)在机械感受器和伤害感受器中表达。 ASIC 通道的作用已在使用具有 ASIC 通道基因靶向缺失的小鼠的行为研究中进行了研究。 ASIC1 的缺失不会改变皮肤机械感受器的功能,但会增加支配肠道的传入神经的机械敏感性。 75 ASIC2 敲除小鼠表现出对快速适应皮肤 LTMR 的敏感性降低。 76 然而,随后的研究报告称,敲除 ASIC2 对内脏机械伤害感受和皮肤机械感觉。 77 ASIC3 中断降低了内脏传入神经的机械敏感性,并降低了皮肤 HTMR 对有害刺激的反应。 76
瞬态受体通道
TRP 超家族在哺乳动物中细分为 78 个亚家族。79 几乎所有 TRP 亚家族的成员都与各种细胞系统中的机械感觉有关。4 然而,在哺乳动物感觉神经元中,TRP 通道以感知热信息和介导神经源性炎症而闻名,只有两个 TRP 通道 TRPV1 和 TRPA4 与触摸响应有关。 扰乱小鼠的 TRPV80,81 表达对急性机械感觉阈值只有适度的影响,但会大大降低对有害机械刺激的敏感性。4 TRPV82,83 是塑造伤害性神经元对渗透压力和炎症期间机械痛觉过敏反应的关键决定因素。1, 1 TRPA1 似乎在机械性痛觉过敏中起作用。 TRPA84,85 缺陷小鼠表现出疼痛过敏。 TRPAXNUMX 有助于伤害感受器感觉神经元中机械、冷和化学刺激的转导,但它似乎对毛细胞转导不是必需的。 XNUMX
没有明确的证据表明哺乳动物中表达的 TRP 通道和 ASIC 通道是机械门控的。 这些异源表达的通道都没有概括在其原生环境中观察到的机械敏感电流的电特征。 这并不排除 ASIC 和 TRP 通道是机械传感器的可能性,因为不确定机械转导通道是否可以在其细胞环境之外发挥作用(参见 SLP3 部分)。
压电蛋白
压电蛋白质最近被 Coste 和合作者确定为机械传感蛋白的有希望的候选者。 86,87 脊椎动物有两个压电成员,压电 1 和压电 2,以前分别称为 FAM38A 和 FAM38B,它们在多细胞真核生物中非常保守. Piezo 2 在 DRGs 中含量丰富,而 Piezo 1 几乎无法检测到。 压电诱导的机械敏感电流被钆、钌红和 GsMTx4(一种来自狼蛛Grammostola spatulata 的毒素)抑制。88 Piezo 1 或 Piezo 2 在异源系统中的表达产生机械敏感电流,Piezo 2 电流的失活动力学更快与压电 1 相似。与内源性机械敏感电流类似,压电相关电流的反转电位约为 0 mV,并且对阳离子没有选择性,Na+、K+、Ca2+ 和 Mg2+ 都渗透到下面的通道中。 同样,压电依赖性电流受膜电位的调节,在去极化电位下电流动力学显着减慢。 86
压电蛋白无疑是机械传感蛋白,并且具有快速适应感觉神经元中的机械敏感电流的许多特性。 用 Piezo 2 短干扰 RNA 处理培养的 DRG 神经元降低了具有快速适应电流的神经元的比例,并降低了机械敏感神经元的百分比。 86 跨膜结构域位于整个压电蛋白中,但没有明显的含孔基序或离子通道特征确定。 然而,小鼠 Piezo 1 蛋白纯化并重组为不对称脂质双层,脂质体形成对钌红敏感的离子通道。87 验证通过压电通道的机械转导的一个重要步骤是使用体内方法来确定触摸信号的功能重要性。 在果蝇中提供了信息,其中单个压电成员的缺失降低了对有害刺激的机械反应,而不影响正常的触摸。 89 虽然它们的结构仍有待确定,但这个新的机械敏感蛋白家族是未来研究的一个有希望的主题,超越国界的触觉。 例如,最近一项针对贫血(遗传性干细胞增多症)患者的研究显示了 Piezo 1 在维持红细胞体积稳态中的作用。 90
跨膜通道样 (TMC)
最近的一项研究表明,两种蛋白质 TMC1 和 TMC2 是毛细胞机械传导所必需的。 91 据报道,人类和小鼠中 TMC1 基因突变导致的遗传性耳聋。 92,93 这些通道的存在尚未在体感系统中显示,但这似乎是一个很好的调查线索。
口腔素样蛋白 3 (SLP3)
除了转导通道外,一些与通道相连的辅助蛋白已被证明在触觉敏感性中发挥作用。 SLP3 在哺乳动物 DRG 神经元中表达。 使用缺乏 SLP3 的突变小鼠进行的研究表明,机械感觉和机械感觉电流发生了变化。94,95 SLP3 的精确功能仍然未知。 它可能是机械敏感通道和底层微管之间的链接器,正如其线虫同源物 MEC2.96 最近 GR 所提出的那样。 Lewin 实验室建议由 DRG 感觉神经元合成一个系链,并将机械敏感离子通道连接到细胞外基质。97 破坏该连接会消除 RA 机械敏感电流,这表明某些离子通道仅在系链时才具有机械敏感性。 RA 机械敏感电流也受到层粘连蛋白 332 的抑制,层粘连蛋白 98 是一种由角质形成细胞产生的基质蛋白,加强了细胞外蛋白调节机械敏感电流的假设。 XNUMX
K+ 通道亚科
与阳离子去极化机械敏感电流平行,正在研究复极化机械敏感 K+ 电流的存在。 机械敏感细胞中的 K+ 通道可以进入当前平衡,并有助于定义机械阈值和机械感受器适应的时间过程。
KCNK 成员属于双孔结构域 K+ 通道 (K2P) 家族。99,100 K2P 显示出由细胞、物理和药理剂调节的显着范围,包括 pH 变化、热、拉伸和膜变形。 这些 K2P 在静息膜电位下是活跃的。 几个 KCNK 亚基在体感神经元中表达。 101 KCNK2 (TREK-1)、KCNK4 (TRAAK) 和 TREK-2 通道是少数通过膜拉伸直接机械门控的通道之一。 102,103
使用 Randall�Selitto 测试,KCNK2 基因被破坏的小鼠表现出对热和轻度机械刺激的敏感性增强,但对施加于后爪的有害机械压力的退缩阈值正常。 104 KCNK2 缺陷小鼠在炎症时也表现出热和机械痛觉过敏增加条件。 KCNK4 敲除小鼠对轻度机械刺激过敏,而这种过敏因 KCNK2.105 的额外失活而增加。XNUMX 这些敲除小鼠的机械敏感性增加可能意味着拉伸通常以协调的方式激活去极化和复极化机械敏感电流,类似于不平衡去极化和复极化电压门控电流。
KCNK18 (TRESK) 是调节体感神经元静息膜电位的背景 K+ 电导的主要贡献者。 106 虽然尚不清楚 KCNK18 是否对机械刺激直接敏感,但它可能在调节对轻触的反应中发挥作用,以及痛苦的机械刺激。 KCNK18 和 KCNK3 在较小程度上被认为是羟基-α-山椒素的分子靶标,羟基山椒素是一种在 Schezuan 花椒中发现的化合物,可激活触觉感受器并在人体中引起刺痛感。 107,108
电压依赖性 K+ 通道 KCNQ4 (Kv7.4) 对于设置小鼠和人类快速适应机械感受器亚群的速度和频率偏好至关重要。 KCNQ4 的突变最初与一种遗传性耳聋有关。 有趣的是,最近的一项研究将 KCNQ4 定位于皮肤快速适应毛囊和迈斯纳小体的周围神经末梢。 因此,KCNQ4 功能的丧失导致机械感受器对低频振动的敏感性选择性增强。 值得注意的是,由于 KCNQ4 基因显性突变而导致迟发性听力损失的人在检测小幅度低频振动方面表现出更高的性能。 109
Alex Jimenez博士的见解
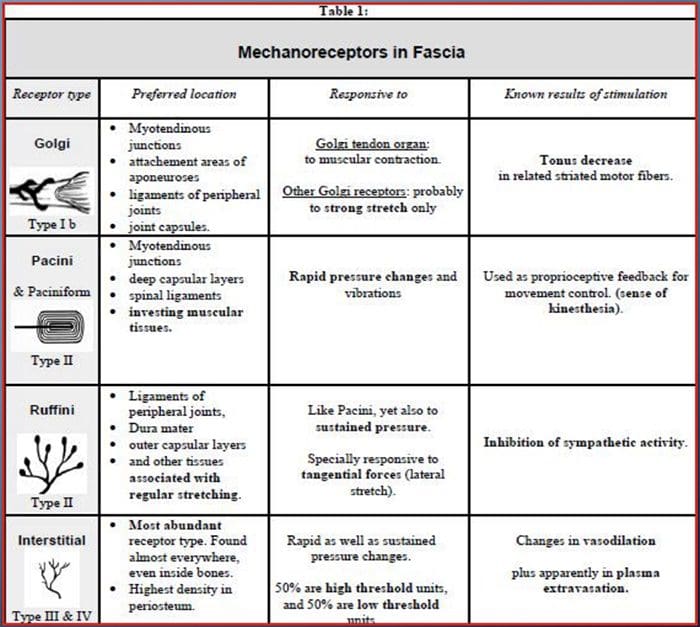
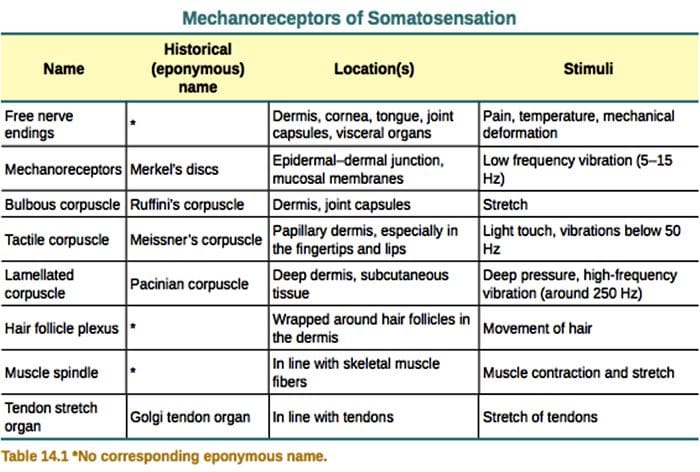
触觉被认为是人体中最复杂的感觉之一,特别是因为没有特定的器官负责它。 相反,触觉是通过称为机械感受器的感觉感受器发生的,这些感受器遍布皮肤并对机械压力或变形作出反应。 在哺乳动物的无毛或无毛皮肤中有四种主要类型的机械感受器:层状小体、触觉小体、默克尔神经末梢和球状小体。 机械感受器的功能是为了检测触摸,以监测肌肉、骨骼和关节的位置,称为本体感觉,甚至检测声音和身体的运动。 了解这些机械感受器的结构和功能机制是利用治疗和疗法进行疼痛管理的基本要素。
结论
触觉是一种复杂的感觉,因为它代表了不同的触觉品质,即振动、形状、质地、愉悦和疼痛,具有不同的辨别表现。 到目前为止,触摸器官与心理物理感觉之间的对应关系是相关的,特定类别的分子标记刚刚出现。 现在需要开发与触摸行为多样性相匹配的啮齿动物测试,以促进未来的基因组学鉴定。 使用缺乏特定感觉传入类型子集的小鼠将极大地促进与特定触摸方式相关的机械感受器和感觉传入纤维的识别。 有趣的是,最近的一篇论文提出了人类机械感觉特征的遗传基础的重要问题,并提出单基因突变可能对触觉敏感性产生负面影响。 110 这强调了人类触觉缺陷的病理生理学在很大程度上是未知的,并且肯定会通过精确识别与触摸方式或触摸缺陷相关的感觉神经元子集来取得进展。
作为回报,在定义机械门控电流的生物物理特性方面取得了进展。 64 近年来新技术的发展,允许监测膜张力变化,同时记录机械门控电流,已证明有价值的实验方法可以描述具有快速、中度和慢速适应的机械敏感电流(在 Delmas 和合作者中进行了评论)。 66,111 未来将确定当前特性在功能多样的机械感受器适应机制中的作用以及机械敏感 K+ 电流对兴奋性的贡献LTMR 和 HTMR。
哺乳动物机械门控电流的分子性质也是一个未来有前途的研究课题。 未来的研究将在两个方面取得进展,首先确定将通道连接到细胞骨架的辅助分子的作用,以及赋予或调节 TRP 和 ASIC/EnaC 家族等离子通道的机械敏感性。 其次,通过回答与渗透和门控机制、感觉神经元子集和涉及压电的触摸方式以及压电在与机械感觉。
与利用特定器官处理这些感觉的视觉、味觉、听觉和嗅觉相比,触觉可以通过称为机械感受器的微小受体发生在全身各处。 不同类型的机械感受器可以在皮肤的各个层中找到,它们可以检测到各种各样的机械刺激。 上面的文章描述了具体的亮点,这些亮点展示了与触觉相关的机械感受器的结构和功能机制的进展。 参考国家生物技术信息中心 (NCBI) 的信息。 我们的信息范围仅限于脊椎按摩疗法以及脊柱损伤和状况。 要讨论主题,请随时询问 Jimenez 博士或通过以下方式联系我们。915-850-0900 。
由Alex Jimenez博士策划
附加主题:腰痛
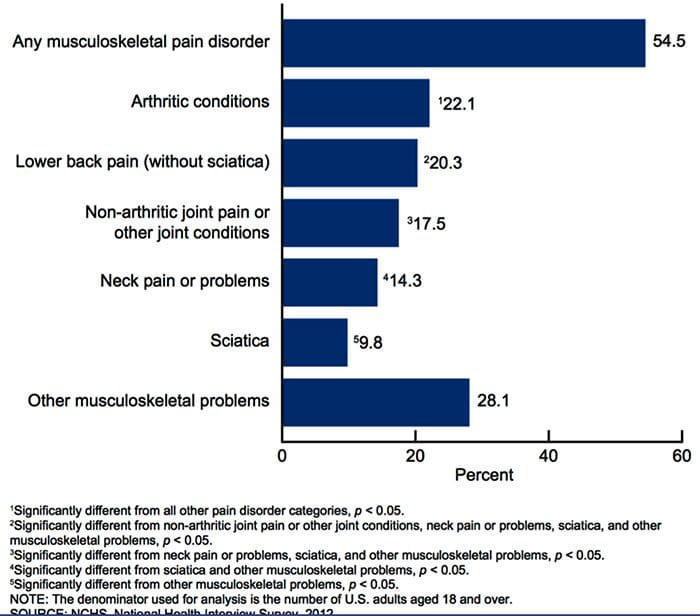
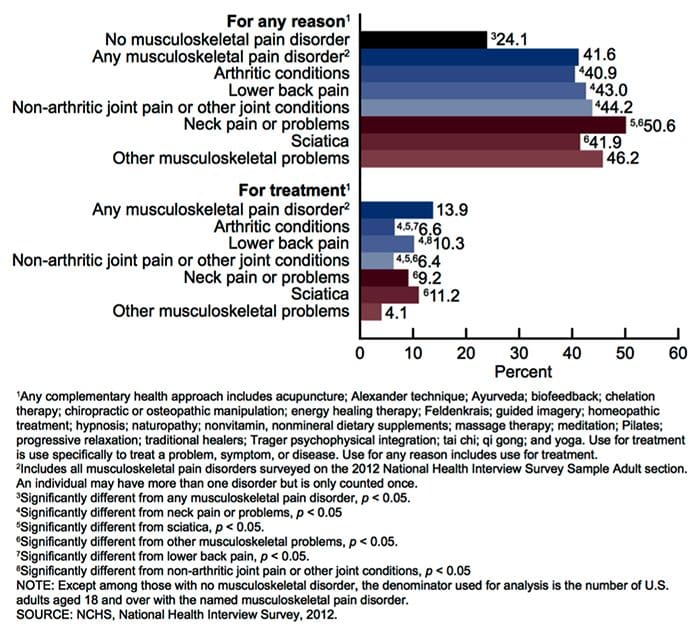
背疼 是造成残障和世界各地缺勤时间最普遍的原因之一。 事实上,背痛被认为是第二次就诊最常见的原因,仅次于上呼吸道感染。 大约80%的人口在一生中至少会经历某种背痛。 脊柱是由骨骼,关节,韧带和肌肉以及其他软组织组成的复杂结构。 因此,受伤和/或病情加重,例如 椎间盘突出 ,最终会导致背部疼痛的症状。 运动伤害或汽车事故伤害通常是造成背痛的最常见原因,但是,有时最简单的动作可能会产生痛苦的结果。 幸运的是,诸如脊椎治疗等替代疗法可以通过使用脊柱调节和手动操作来帮助缓解背部疼痛,最终改善疼痛缓解。
VIDEO
VIDEO

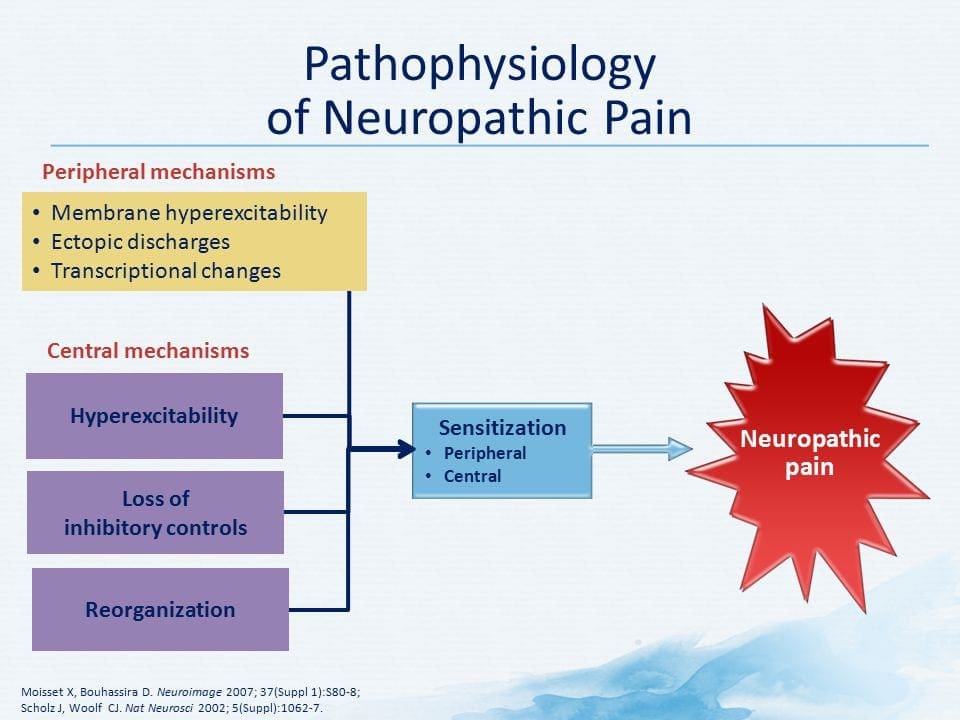
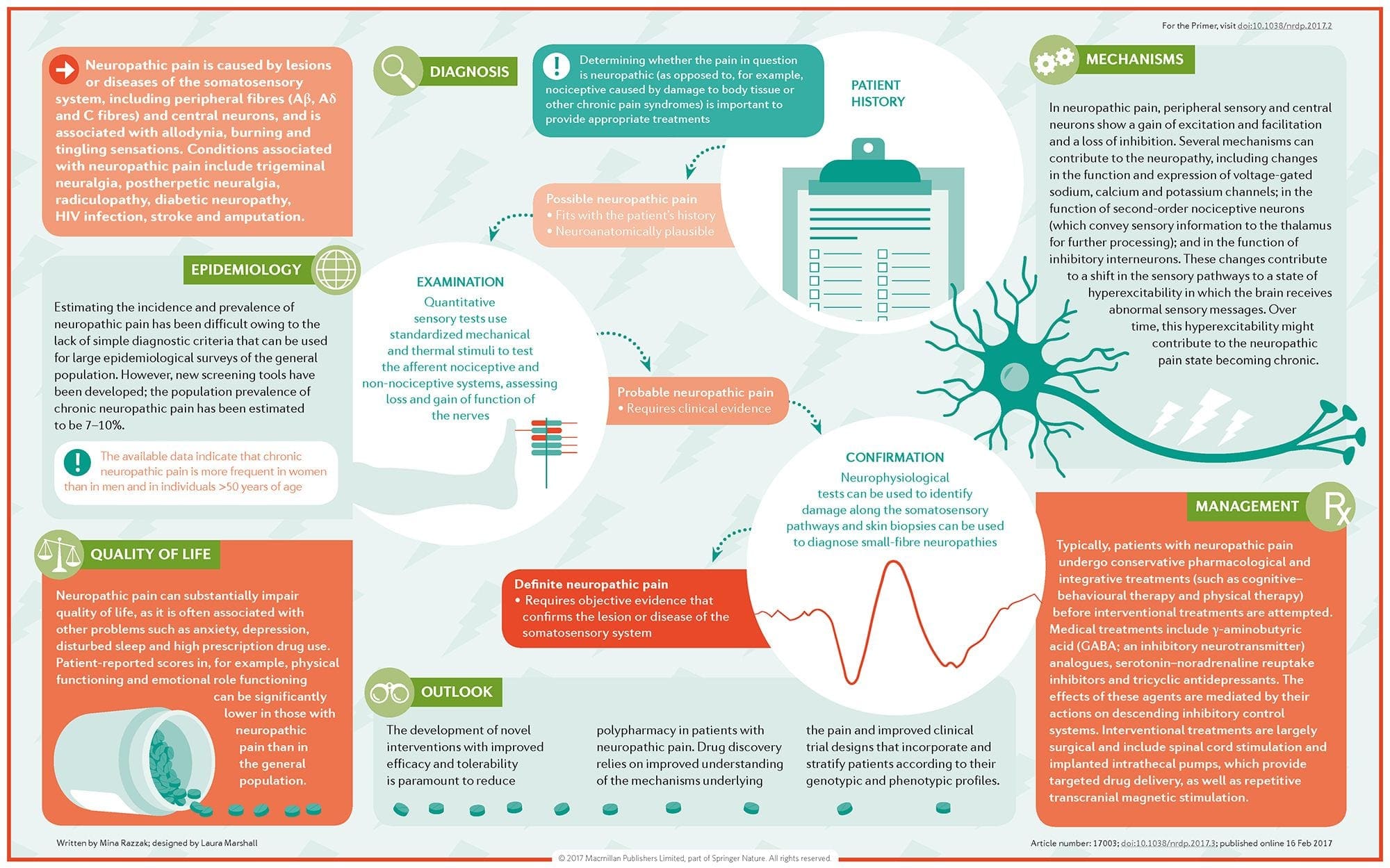


































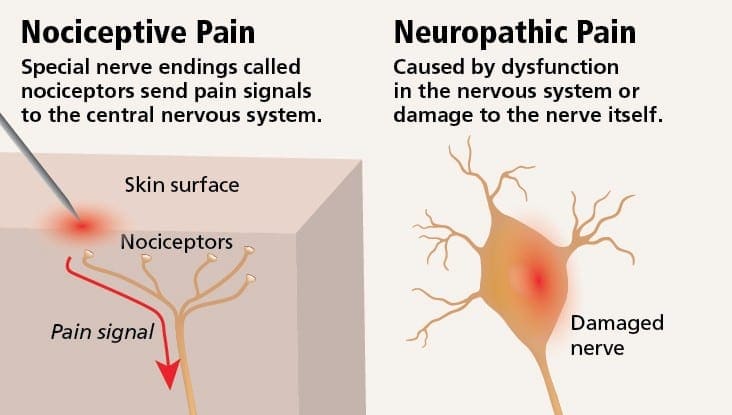
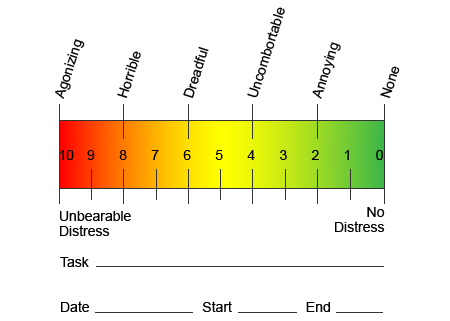


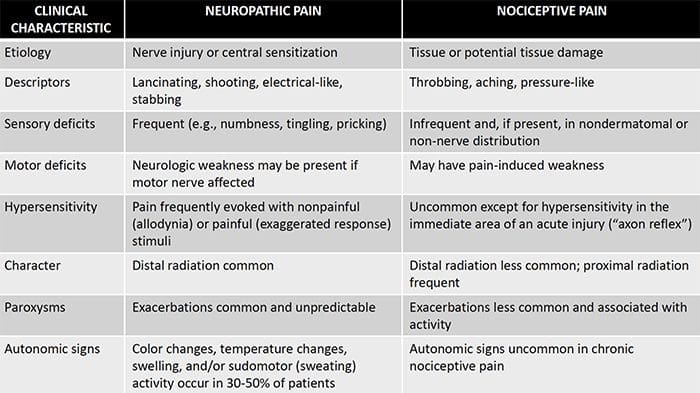
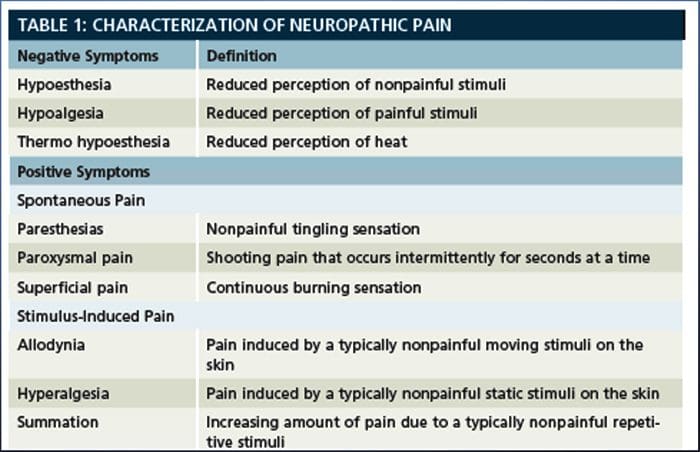
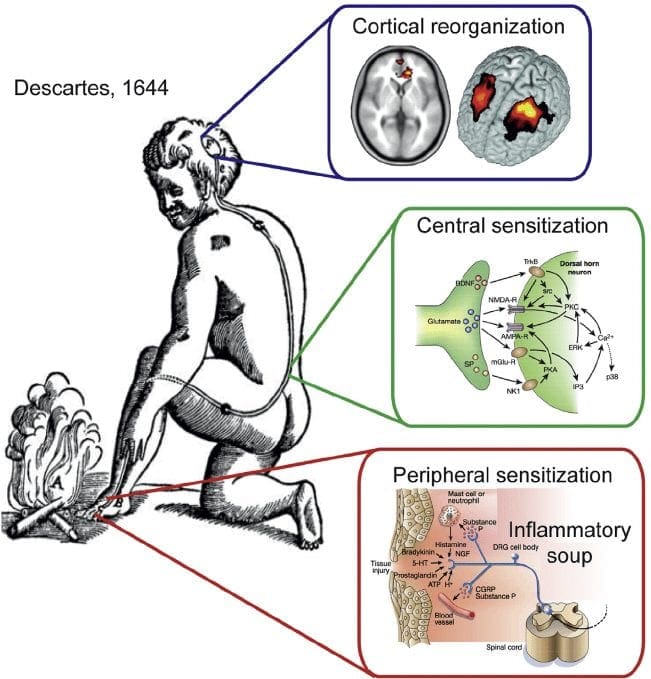
 神经性疼痛的发病
神经性疼痛的发病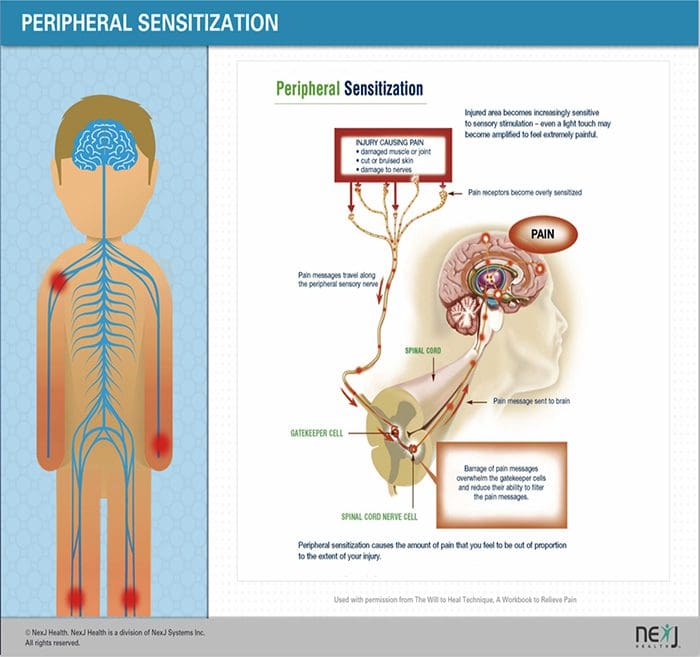
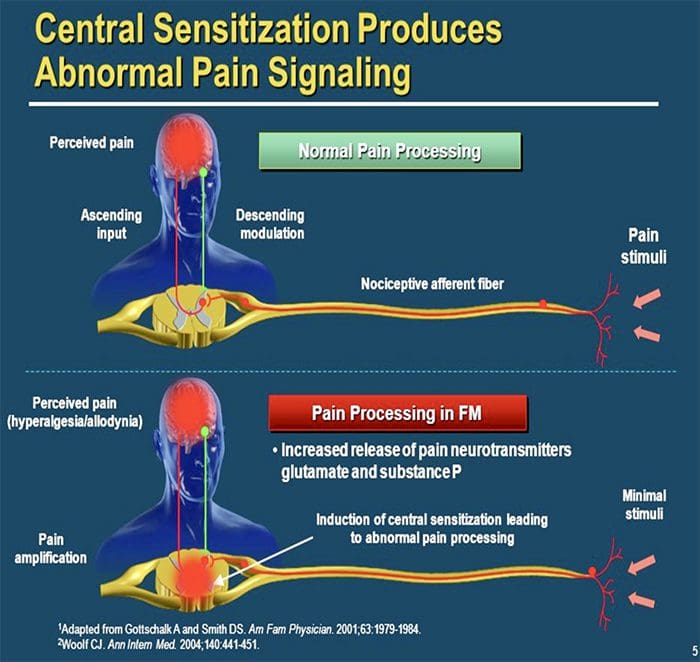
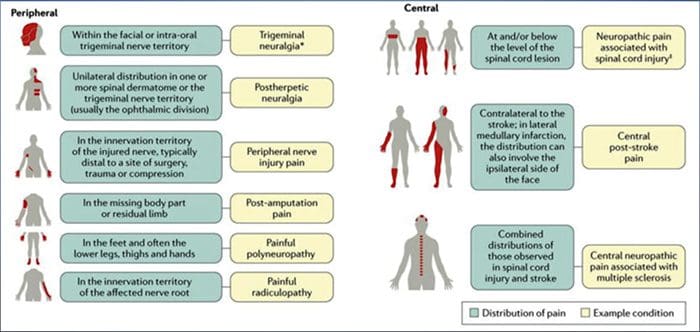 常见原因
常见原因





 幻肢痛和增强现实
幻肢痛和增强现实
 常见原因
常见原因



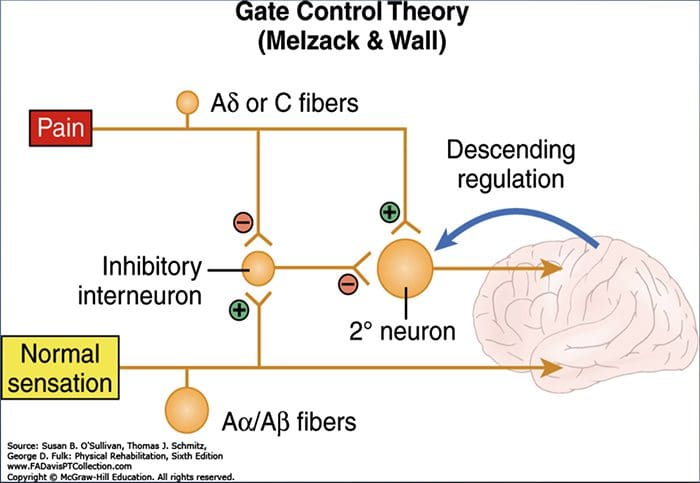
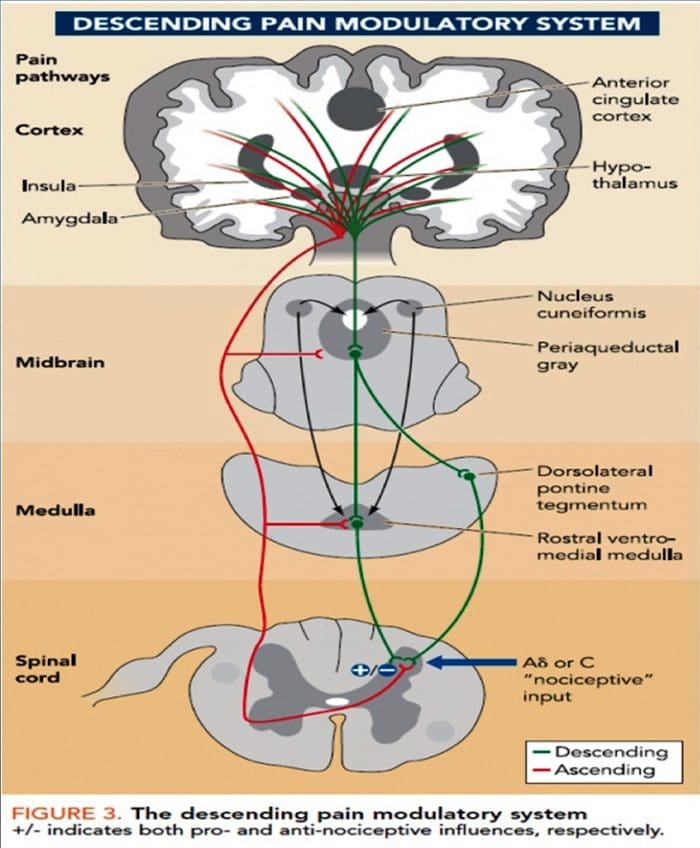
 门控疼痛理论
门控疼痛理论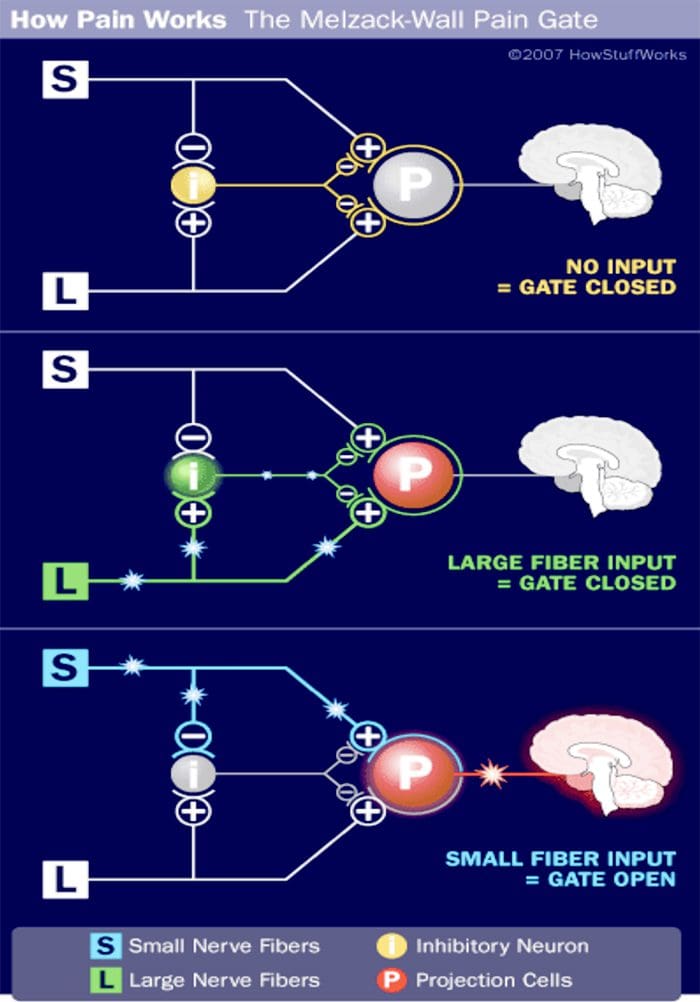
 背侧柱内侧 LEMNISCAL 通路
背侧柱内侧 LEMNISCAL 通路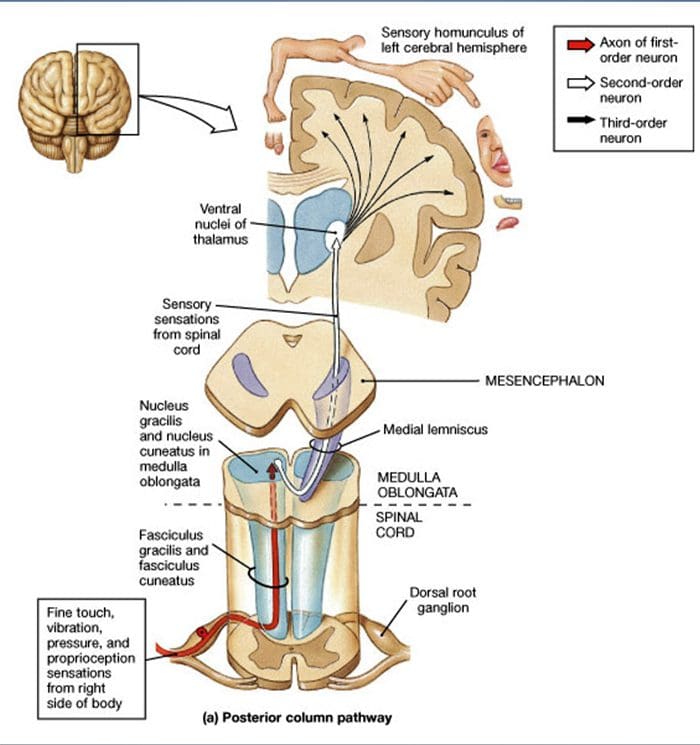 利用外周机械感受器改变疼痛感知
利用外周机械感受器改变疼痛感知
 振动
振动
 轻触
轻触





 客户案例
客户案例 体检要点
体检要点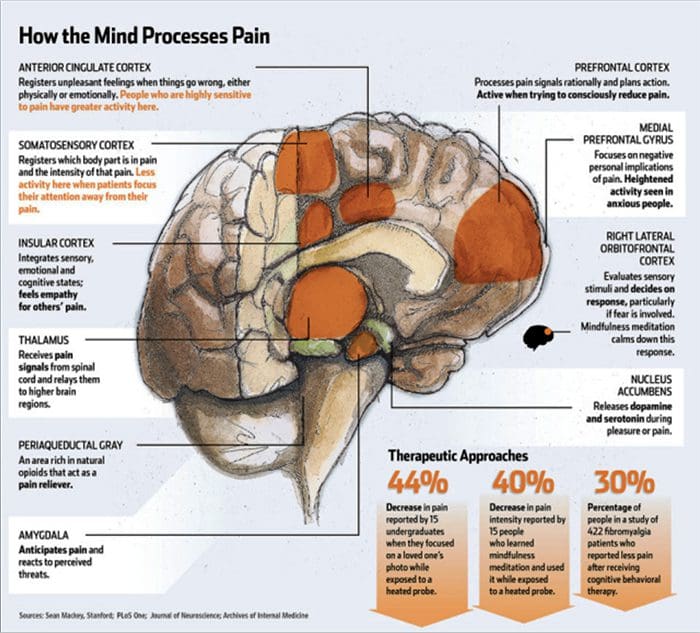 体检要点
体检要点
 两天后
两天后